
| A.制取NF3的反应中,氧化剂与还原剂的物质的量之比为3∶1 |
| B.在NF3与H2O的反应中,H2O作还原剂 |
| C.若在制取NF3的反应中有0.5 mol NH3参加反应,转移电子的物质的量为3 mol |
| D.NF3在空气中一旦泄漏,不易于发现 |
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.NH4CuSO3中硫元素被氧化了 | B.刺激性气味的气体是二氧化硫或氨气 |
| C.该反应中NH4CuSO3既是氧化剂又是还原剂 | D.该反应中硫酸既表现为酸性又表现氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
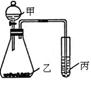
| 实验试剂 | 实验结论 | ||
| 甲 | 乙 | 丙 | |
| ① | 高锰酸钾 | ② | 氧化性:KMnO4>Cl2>Br2 |
 (1)图中①为 ,②为 。
(1)图中①为 ,②为 。 (2)请你根据上述实验装置再设计一个实验,并将选择的试剂、丙中的现象以及根据实验现象得出的实验结论填入下表;
(2)请你根据上述实验装置再设计一个实验,并将选择的试剂、丙中的现象以及根据实验现象得出的实验结论填入下表;| 试剂甲 | 试剂乙 | 试剂丙 | 丙中现象 | 实验结论 |
| | | | | 酸性:盐酸>碳酸 |
| | | 石蕊试液 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 X+H2 ③Y+NaOH→G+W+H2O
X+H2 ③Y+NaOH→G+W+H2O | A.W、G、Z、Y、X | B.G、Y、W、Z、X |
| C.G、Y、Z、W、X | D.Z、X、G、Y、W |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2↑+Cl2↑ ______________________________
H2↑+Cl2↑ ______________________________查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com