
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:推断题
 ,C微粒的结构示意图为
,C微粒的结构示意图为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 锡、铅均是第ⅣA 族元素.在溶液中Pb2+很稳定而为Pb4+不稳定.
锡、铅均是第ⅣA 族元素.在溶液中Pb2+很稳定而为Pb4+不稳定.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1.6 g O2和O3混合气体中原子总数为0.1NA | |
| B. | 标准状况下,过氧化钠与水反应生成1.12 L氧气时转移电子数目为0.2NA | |
| C. | 0.1 mol•L的CH3COONa溶液中CH3COOH和CH3COO-总数为0.1NA | |
| D. | 常温常压下,4 g He中,含有的原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

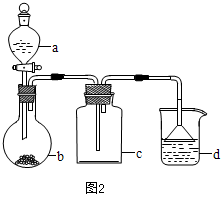
| 选项 | a物质 | b物质 | c收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A1Cl3 | B. | Na2O | C. | Na(Al(OH)4) | D. | SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO+2HCl═CuCl2+H2O | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | Zn+H2SO4═ZnSO4+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据结构相似的分子的熔点与相对分子质量的关系,推出PH3比NH3熔点高 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com