
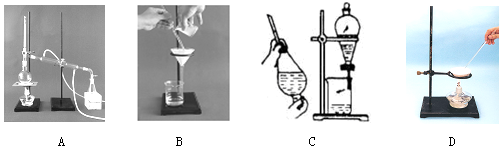
分析 (1)CaCO3不溶于水;
(2)碘不易溶于水,易溶于有机溶剂;
(3)自来水中水的沸点低;
(4)植物油和水分层;
(5)海水中水的沸点低,盐的沸点高.
解答 解:由装置可知,A为蒸馏装置、B为过滤装置,C为分液、萃取,D为蒸发装置,
(1)CaCO3不溶于水,则选择过滤法分离,故答案为:B;
(2)碘不易溶于水,易溶于有机溶剂,则选择萃取、分液分离,故答案为:C;
(3)水的沸点低,则选择蒸馏法制备蒸馏水,故答案为:A;
(4)植物油和水分层,选择分液法分离,故答案为:C;
(4)海水中水的沸点低,盐的沸点高,与蒸发原理相同,故答案为:D.
点评 本题考查混合物分离提纯,为高频考点,把握实验装置的作用、混合物分离提纯为解答的关键,侧重分析与实验能力的考查,注意分离方法的选择,题目难度不大.


科目:高中化学 来源: 题型:解答题
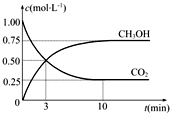 “低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为283kJ | |
| B. | 25℃、101 kPa时,1 mol CO和2 mol CO的燃烧热相等 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452 kJ/mol | |
| D. | CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0×10-7mol•L-1 | B. | 0.1×10-7mol•L-1 | C. | 5.0×10-6mol•L-1 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
 ,含有的化学键类型离子键和共价键,Z2Y2为离子晶体.
,含有的化学键类型离子键和共价键,Z2Y2为离子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用84消毒液除去地砖上的有色物质 | |
| B. | 用米汤检验加碘盐中的碘酸钾(KIO3) | |
| C. | 用纯碱(Na2CO3)溶液洗涤沾有油污的器具 | |
| D. | 利用燃烧的方法鉴别蚕丝和棉花 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ④⑤ | D. | ④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com