
| V |
| 22.4L/mol |
| m |
| ρ |
| n |
| V |
| aL |
| 22.4L/mol |
| a |
| 22.4 |
| a |
| 22.4 |
| 17a |
| 22.4 |
| 17a |
| 22.4 |
1000g+
| ||
| bg/L |
| 22400+17a |
| 22.4b |
| ||
|
| 17ab |
| 22400+17a |
| 17ab |
| 22400+17a |
| 17a |
| 22.4 |
| a |
| 22.4 |
| 17a |
| 22.4 |
| ||
1000g+
|
| 1700a |
| 22400g+17a |
| 1700a |
| 22400g+17a |


科目:高中化学 来源: 题型:
| A、Fe3+>HClO>Cl2>Fe2+>Cu2+ |
| B、HClO>Cl2>Fe3+>Cu2+>Fe2+ |
| C、Cl2>HClO>Fe3+>Cu2+>Fe2+ |
| D、HClO>Fe3+>Cl2>Cu2+>Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液物质的量浓度因溶液的密度未知而无法求得 |
| B、该溶液中溶质的质量分数因溶液的密度未知而无法求得 |
| C、该溶液物质的量浓度为10 mol.L-1 |
| D、所得溶液的体积为22.5L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150 mL 1 mol?L-1的NaCl |
| B、75 mL 2 mol?L-1的NH4Cl |
| C、150 mL 3 mol?L-1的KCl |
| D、75 mL 2 mol?L-1的CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积相同,但不一定是22.4L |
| B、分子数相同,但原子数不同 |
| C、摩尔质量不同,但质量相同 |
| D、质子数不同,电子数也不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.4g金属镁所含电子数目为0.2NA |
| B、16gCH4所含原子数目为NA |
| C、17gNH3所含电子数目为NA |
| D、18g水所含分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸与氯化钡反应:SO42-+Ba2+=BaSO4↓ |
| B、碳酸钙放入稀盐酸中:CO32-+2H+=CO2↑+H2O |
| C、稀硫酸滴在锌片上:Zn+2H+=Zn2++H2↑ |
| D、CuO和盐酸反应:CuO+2H+=Cu2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
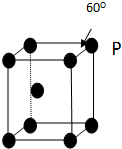 A、B、C、D、E五种元素其核电荷数依次增大.A原子只有1个s电子,B原子L层中s电子和p电子数目相同,B、C、D属于同周期且相邻,E原子内层均饱和,N层上只有两个电子.
A、B、C、D、E五种元素其核电荷数依次增大.A原子只有1个s电子,B原子L层中s电子和p电子数目相同,B、C、D属于同周期且相邻,E原子内层均饱和,N层上只有两个电子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com