
| A、二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| B、碳酸氢钠具有弱酸性,可用于食品发酵 |
| C、次氯酸钠具有强氧化性,可用于配制消毒液 |
| D、明矾能水解生成Al(OH)3胶体,可用作净水剂 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、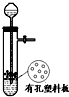 用于Cu和浓H2SO4反应制取少量的SO2气体 |
B、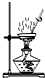 用于灼烧Al(OH)3 |
C、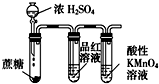 用于检验浓硫酸与蔗糖反应产生的二氧化硫 |
D、 由于实验室制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 用亚硫酸溶液无法制取硫酸溶液 |
| B | 升高温度,反应速率越快 | 常温下钠与氧气反应生成氧化钠,升高温度,Na2O的生成速率加快 |
| C | 金属越活泼,其阳离子氧化性越弱 | Fe3+的氧化性弱于Cu2+ |
| D | Ksp小的沉淀易向Ksp更小的沉淀转化 | CaSO4悬浊液中滴加Na2CO3溶液可生成CaCO3沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、玻璃、水泥、陶瓷都是硅酸盐产品 |
| B、水晶、玛瑙的主要成分都是SiO2 |
| C、硅元素在地壳中含量最多 |
| D、二氧化硅和大多数硅酸盐的化学性质都很稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中性溶液:Cu2+、Al3+、NO3-、SO42- |
| B、加入苯酚显紫色的溶液:K+、NH4+、Cl-、NO3- |
| C、加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- |
| D、常温下,c(H+)/c(OH-)=1×1012的溶液:K+、AlO2-、CO32-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 氯化钠是电解质 | 电解氯化钠溶液可制备金属钠 |
| B | CO2是酸性氧化物 | CO2通入CaCl2溶液可得到CaCO3沉淀 |
| C | 常温下浓硫酸的强氧化性使铝钝化 | 可用铝罐槽车储运浓硫酸 |
| D | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
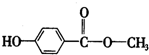 下列说法中正确的是( )
下列说法中正确的是( )| A、在一定条件下,1 mol该物质最多能和2 mol NaOH反应 |
| B、该物质属于芳香烃 |
| C、该物质不能够和FeCl3反应 |
| D、该物质的分子式为C8H10O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com