��2012?������ģ�����������е�β������ɻ�����Ⱦ���[���������տ�������ȾԴ�����������Դ����֪��
��Fe
2O
3��s��+3CO��g��?2Fe��s��+3CO
2��g����H=-25kJ/mol
��3Fe
2O
3��s��+CO��g��?2Fe
3O
4��s��+CO
2��g����H=-47kJ/mol
��Fe
3O
4��s��+CO��g��?3FeO��s��+CO
2��g����H=+19kJ/mol
��1���Լ��㷴Ӧ��FeO��s��+CO��g��?Fe��s��+CO
2��g����H=
-11kJ/mol
-11kJ/mol
��
��2����֪1092��ʱ��1���з�Ӧ��ƽ�ⳣ��Ϊ0.35����1L���ܱ������У�Ͷ��7.2gFeO��0.1mol CO���ȵ�1092�沢���ָ��¶ȣ���Ӧ��t
1ʱ��ƽ�⣮
��t
1ʱ��Ӧ��ƽ���CO������������Ϊ
74%
74%
��

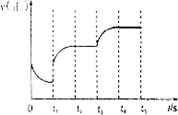
�ڸ÷�Ӧ������Ӧ������ʱ��仯�����ͼ����ʾ����t
1ʱ�ı���ij����������Ӧ��t
2ʱ��ƽ�⣬�ı������������
a
a
a�������¶� b������CO��Ũ��
c��ʹ�ô��� d������ѹǿ
�������t
3ʱ������CO
2������t
4ʱ��Ӧ�ִ�����ƽ��״̬�����ڼ�ͼ�ϻ���t
3��t
5ʱ��ε�v�������仯����
��
��3������β��������ֱ��������̼����ȼ�ϵ�أ�����ԭ����ͼ�ң���ȼ�ϣ����ĵ�Q��ӦΪ
CO+CO32--2e-�T2CO2
CO+CO32--2e-�T2CO2
��
��4��ת¯���֣�β����CO���������58%-70%��ij�ֳ�����NaOH����CO���ɼ����ƣ�������SO
2���ɱ��շۣ�Na
2S
2O
4������д�������ƺ��������ƻ����Һ��SO
2���ɱ��շ�ͬʱ���ɶ�����̼�����ӷ���ʽ
HCOO-+OH-+2O2�TS2O42-+H2O+CO2
HCOO-+OH-+2O2�TS2O42-+H2O+CO2
��
��5��Ŀǰ�ҹ��������ҵ�ǽ�CO��ˮ������Ӧת��ΪH
2��Ȼ����H
2��N
2��Ӧ�ϳɰ������ռ�����״����3360m
3β��������CO�������Ϊ60%������ѭ���������ٶ�����ת���ʾ�Ϊ100%�������Ͽɻ��NH
31.02
1.02
t��



 ��
�� ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
 ��2012?������ģ����֪������C6H6��������B3N3H6�������ķ��ӽṹ���ƣ���ͼ�����Ķ���ȡ����B3N3H4Cl2��ͬ���칹�����ĿΪ��������
��2012?������ģ����֪������C6H6��������B3N3H6�������ķ��ӽṹ���ƣ���ͼ�����Ķ���ȡ����B3N3H4Cl2��ͬ���칹�����ĿΪ��������