
���� ��1����������ƿû��480mL�ģ�����Ҫ����500mL 0.1mol/L������ͭ��Һ��
��2�����ݲ��������ܽ����ʡ���Һ���������ý��
��3������n=CV��m=nM������Ҫ CuSO4•5H2O��������
��4������c=$\frac{n}{V}$����������������n��V��Ӱ�죬���nƫ���VƫС������������ҺŨ��ƫ�ߣ�
��5�����ݲ��õ��ǽ�ͷ�ιܣ�������ƿ�������ˮ����̶���1-2cm��ֹͣ�����ý�ͷ�ιܼ�����ˮ����Һ��Һ��������̶������У�
��� �⣺��1������ƿû��480mL�ģ�����Ҫ����500mL 0.1mol/L������ͭ��Һ���ʴ�Ϊ��500��
��2�����������ܽ����ʲ����������ǽ��裬���ٹ����ܽ⣻����Һ�����е������ǣ��������ʴ�Ϊ�����裬���ٹ����ܽ⣻ ������
��3��ʵ����������480mL0.1mol/L��CuSO4��Һ����Ҫѡ��500mL����ƿ��ʵ�������Ƶ���500mL 0.1mol/L������ͭ��Һ����Ҫ����ͭ�����ʵ���Ϊ��0.1mol/L��0.5L=0.05mol����Ҫ����ͭ��������160g/mol��0.05mol=8.0g����Ҫ��ˮ����ͭ���������Ϊ��250g/mol��0.05mol=12.5g���ʴ�Ϊ��12.5��
��4����������ƿϴ����δ�����������ˮ������c=$\frac{n}{V}$���������n��V��û��Ӱ�죬��Ӱ����������ҺŨ�ȣ��ʴ�Ϊ����Ӱ�죻
�ڶ���ʱ�����۾����ӣ�����c=$\frac{n}{V}$����������Vƫ�٣��������Ƶ���ҺŨ�Ƚ�ƫ�ߣ��ʴ�Ϊ��ƫ�ߣ�
��5��������ƿ�������ˮ����̶���1-2cm��ֹͣ�����ý�ͷ�ιܼ�����ˮ����Һ��Һ��������̶������У��ʴ�Ϊ����ͷ�ιܣ�
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƹ��̡������Լ����������ѶȲ���ע��ʵ��Ļ�������������ע�����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
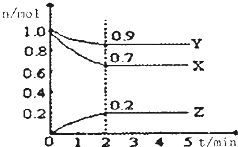 ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ���ݴ˻ش�
ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ���ݴ˻ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4 mol A+2 mol B | B�� | 3 mol C+2 mol D | ||
| C�� | 1 mol B+3 mol C+1 mol D | D�� | 2 mol A+1 mol B+3mol C+1 mol D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
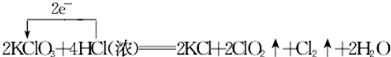 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
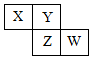 X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����Zԭ�ӵ������������ǵ�һ���������3��������˵����ȷ���ǣ�������
X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����Zԭ�ӵ������������ǵ�һ���������3��������˵����ȷ���ǣ�������| A�� | Y������������Ӧ��Z���� | |
| B�� | ����������Ӧˮ��������W��Z�� | |
| C�� | X����������ǿ��Y���� | |
| D�� | X��W��ԭ�Ӻ�����������9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 200mL 2 mol/LMgCl2��Һ | B�� | 1000mL 2.5 mol/L NaCl��Һ | ||
| C�� | 300mL 5 mol/L KCl��Һ | D�� | 250mL 1 mol/L FeCl3��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com