
 c��Cl-��=
c��Cl-��= ��0.2mol/L=0.1mol/L���ʴ�Ϊ��0.1mol/L��
��0.2mol/L=0.1mol/L���ʴ�Ϊ��0.1mol/L��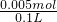 =0.05mol/L��
=0.05mol/L�� c��Cl-����
c��Cl-����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�긣��ʡ�������谲һ�и�һ��ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
ij100mL��CuCl2��Һ�У���֪��Һ�е�Cl����Ũ��Ϊ0.2 mol��L��1���ֽ�һ����������Ͷ�뵽����Һ�У��ش��������⣺
��1��ԭ��Һ��Cu2+��Ũ��Ϊ������������������������
��2����Ӧ����Cl����Ũ��Ϊ����������������������mol��L��1��
��3������Ӧ����Fe2+����ҺΪ0.05 mol��L��1����Ӧ����ͭ���ʵ�����Ϊ���� ����g��
��4��ʣ���Cu2+��Ũ��Ϊ������ ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�긣��ʡ�ĵ���У��һ�������¿���ѧ�Ծ����������� ���ͣ������
��11�֣�
��������ȵ�O3��O2�У����Ӹ���֮��Ϊ___________��ԭ�Ӹ���֮��Ϊ____________��
���������ͬ�¶Ⱥ���ͬѹǿ�����£�O3Ϊ���壩O3��O2�������Ϊ___ ________��
��ij100mL��CuCl2��Һ�У���֪��Һ�е�Cl����Ũ��Ϊ0.2mol/L���ֽ�һ����������Ͷ�뵽����Һ�У���������Һ������仯�����ش��������⣺
��1��ԭ��Һ��Cu2+�����ʵ���Ũ��Ϊ������������������������
��2����Ӧ����Cl�������ʵ���Ũ��Ϊ�������������������� ��
��3������Ӧ����Fe2+����ҺΪ0.05mol/L����Ӧ����ͭ���ʵ�����Ϊ����������
��4��ʣ���Cu2+�����ʵ���Ũ��Ϊ�������� ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com