
| 元素 | A | B | C | D | E |
| 结构或性质 | 原子半径最小的元素 | 地壳中含量最多的元素 | 可与B形成阴阳离子个数比为1:2的两种化合物 | 与B同主族 | 单质是生活中最常见的金属,可被磁铁吸引 |
 2H2O+O2↑和 。若在X极收集气体672 mL,在Y极收集气体168 mL(均已折算为标况下体积),则Y电极质量减少 g。
2H2O+O2↑和 。若在X极收集气体672 mL,在Y极收集气体168 mL(均已折算为标况下体积),则Y电极质量减少 g。
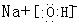 ;Na2S、NaHS、Na2SO3
;Na2S、NaHS、Na2SO3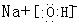 ;乙能促进水的电离,说明乙是水解显碱性的盐,所以乙为硫化钠Na2S、硫氢化钠NaHS、亚硫酸钠Na2SO3,
;乙能促进水的电离,说明乙是水解显碱性的盐,所以乙为硫化钠Na2S、硫氢化钠NaHS、亚硫酸钠Na2SO3,

 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源:不详 题型:单选题
| A.五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B.化合物X2W2、YW2、ZW2等都含有极性共价键和非极性共价键 |
| C.用M单质作阳极,石墨电极作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
| D.X、Z两元素能形成原子个数比为3∶1和4∶2的化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HF的稳定性比HCl强 |
| B.Mg失电子能力比Ca弱 |
| C.NaCl与NH4Cl含有的化学键类型相同 |
| D.等物质的量的H2S和H2O2含电子数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.57 | B.47 | C.61 | D.293 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.高氯酸的酸性比亚硫酸强 | B.次氯酸的氧化性比稀硫酸强 |
| C.氯化氢比硫化氢的热稳定性好 | D.氯原子最外层电子数比硫原子多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.硫原子的原子结构示意图: |
B.NH4Cl的电子式: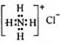 |
C.原子核内有10个中子的氧原子: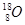 |
| D.纯碱的化学式为NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素的相对原子质量是小数,是由于元素具有同位素 |
| B.有相同质子数的原子或离子一定属于同种元素 |
| C.K+和Ar具有相同的电子层结构,氧化性K+比Ar强 |
| D.金属离子的电子层数一定比金属原子的电子层数少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com