
| A、金属钠要保存在煤油中 |
| B、金属铝的熔点高,常作为耐高温的材料 |
| C、氢氧化亚铁是白色絮状沉淀,在空气中变成灰绿色,最终会变成红褐色 |
| D、小苏打、氢氧化铝都可以治疗胃酸过多 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 科学家利用太阳能分解水生成氢气,再用氢气与二氧化碳在催化剂作用下反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知:
科学家利用太阳能分解水生成氢气,再用氢气与二氧化碳在催化剂作用下反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K2CO3 HCl CaCl2 |
| B、Na2CO3 HNO3 MgCl2 |
| C、Na2CO3 HCl AgNO3 |
| D、H2SO4 Na2CO3 AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业利用上述信息,按图所示的路线合成物质M(结构简式如右图所示),该物质是一种香料.
工业利用上述信息,按图所示的路线合成物质M(结构简式如右图所示),该物质是一种香料.
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径
,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径
 和
和查看答案和解析>>
科目:高中化学 来源: 题型:
 反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A、A、C两点的NO2的体积分数:C>A |
| B、A、C两点气体的颜色:A深,C浅 |
| C、由状态B到状态A,可以用加热的方法 |
| D、若p2>p1,则化学平衡常数KA>KC |
查看答案和解析>>
科目:高中化学 来源: 题型:
 它的合成路线如下:
它的合成路线如下:
 中除硫醚键(-S-)外,还含有的官能团名称
中除硫醚键(-S-)外,还含有的官能团名称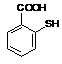 一定条件下形成聚合物的结构简式为
一定条件下形成聚合物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
 -CH3)
-CH3)  -CH3)
-CH3) -CH=CH2)
-CH=CH2)  -C2H5)
-C2H5)

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在3mL甲酸浓溶液中加入2滴新制氢氧化铜,加热来检验醛基 |
| B、用加入过量氢氧化钠溶液,振荡、分液的方法除去苯中混有的苯酚杂质 |
| C、将铁屑、溴水、苯混合以制取溴苯 |
| D、除去乙烷中少量的乙烯的方法是:光照条件下通入Cl2,气、液分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com