
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.常温常压下,17 g甲基(—14CH3)所含的中子数为9NA
B.pH=1的稀硫酸中含有的H+数为0.1NA
C.7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA
D.3 mol NO2和足量H2O反应,转移NA个电子
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2014高考化学专题突破训练 专题8电化学原理练习卷(解析版) 题型:选择题
下列叙述中,不正确的是( )
A.原电池是将化学能转化为电能的装置
B.轮船底部镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁腐蚀的负极反应:Fe-3e-=Fe3+
D.电镀时,镀层金属作阳极,镀件作阴极
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题4化学反应中的能量变化练习卷(解析版) 题型:填空题
(1)如图表示金刚石、石墨在相关反应过程中的能量变化关系。
写出石墨转化为金刚石的热化学方程式 。
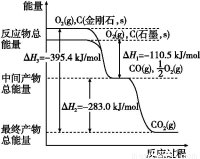
(2)已知:Ti(s)+2Cl2(g) TiCl4(l)ΔH=-804.2 kJ/mol
TiCl4(l)ΔH=-804.2 kJ/mol
2Na(s)+Cl2(g)=2NaCl(s) ΔH=-882.0 kJ/mol
Na(s)=Na(l) ΔH=+2.6 kJ/mol
则TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s)的ΔH= kJ/mol。
(3)已知:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH=-a kJ/mol
②CH3OH(l)+O2(g)=CO(g)+2H2O(l)ΔH=-b kJ/mol
③H2O(g)=H2O(l) ΔH=-c kJ/mol则:2CO(g)+O2(g) 2CO2(g)的ΔH= kJ/mol。
2CO2(g)的ΔH= kJ/mol。
(4)工业上在催化剂作用下可利用CO合成甲醇:CO(g)+2H2(g)=CH3OH(g),下图表示反应过程中能量的变化情况。
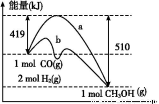
在图中,曲线 (填“a”或“b”)表示使用了催化剂;该反应属于 (填“吸热”或“放热”)反应。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题3氧化还原反应 离子反应练习卷(解析版) 题型:选择题
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存说法中正确的是( )
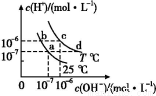
A.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、S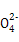
B.b点对应的溶液中大量存在:N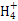 、Ba2+、OH-、I-
、Ba2+、OH-、I-
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HC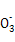
D.d点对应的溶液中大量存在:Na+、K+、S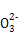 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题2化学常用计量 溶液练习卷(解析版) 题型:选择题
若用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A.1 mol BrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA
B.锌与一定浓度的浓硫酸反应,产生标准状况下SO2和H2的混合气体22.4 L,锌失去电子数为2NA
C.常温常压下,20 g D2O含有的原子总数为3NA
D.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数小于2NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题1物质的组成性质分类和化学用语练习卷(解析版) 题型:选择题
分类法是学习化学的重要方法,人们在认识事物时可采用多种分类方法。下列各组分类中不合理的是( )
选项分类标准物质(反应)
归类
AFeSO4、NO2、MnO2、NaClO、Cu3P、Na2O2H2SO3
BCH3COOH、HOOC—COOH、HClO、H2SHF
C复分解反应、电解反应、放热反应、离子反应焰色反应
D(NH4)2SO4、NH4Cl、NH4NO3、NH3·H2ONH4HCO3
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题1物质的组成性质分类和化学用语练习卷(解析版) 题型:选择题
只含有一种元素的物质( )
A.可能是纯净物也可能是混合物
B.可能是单质也可能是化合物
C.一定是纯净物
D.一定是一种单质
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题13物质结构与性质选修3练习卷(解析版) 题型:填空题
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态Ni原子的价电子(外围电子)排布式为 ;
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 ;
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③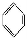 、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形;
、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形;
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”);
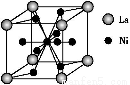
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。该合金的化学式为 ;
查看答案和解析>>
科目:高中化学 来源:2014江苏省扬州市届高三上学期期末考试化学试卷(解析版) 题型:填空题
以粗氧化锌粉(含FeO、Fe2O3、ZnS等)制取活性ZnO的工艺如下:
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品。
已知:离子沉淀的pH见下表。
离子 | 开始沉淀pH | 沉淀完全pH |
Fe2+ | 7.6 | 9.6 |
Fe3+ | 2.7 | 3.7 |
Zn2+ | 5.4 | 8.0 |
(1)加入H2O2时能浸出硫化锌,同时生成淡黄色固体,写出其化学方程式 。
(2)步骤2中调节溶液pH的范围是 。
(3)取洗涤、干燥后的碱式碳酸锌68.2 g,充分灼烧后测得残留物质的质量为48.6 g,将所得气体通入足量澄清石灰水中,得沉淀20 g。计算碱式碳酸锌的组成(用化学式表示,写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com