
| A.△H<0、△S>0 | B.△H<0、△S<0 |
| C.△H>0、△S>0 | D.△H>0、△S<0 |
科目:高中化学 来源:不详 题型:单选题
 C(s)+1/2O2(g)的△H为正值,△S为负值。若△H和△S随温度的变化忽略不计,下列说法中正确的是 ( )
C(s)+1/2O2(g)的△H为正值,△S为负值。若△H和△S随温度的变化忽略不计,下列说法中正确的是 ( )| A.低温下反应是自发进行,高温下反应是非自发进行 |
| B.任何温度下反应都是自发进行 |
| C.低温下反应是非自发进行,高温下反应是自发进行 |
| D.任何温度下反应都是非自发进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 A2(g)+3B2(g);ΔH>0 (图中AB3%为体系中AB3的体积百分含量,v为反应速率)。关于该可逆反应的下列图象不正确的是
A2(g)+3B2(g);ΔH>0 (图中AB3%为体系中AB3的体积百分含量,v为反应速率)。关于该可逆反应的下列图象不正确的是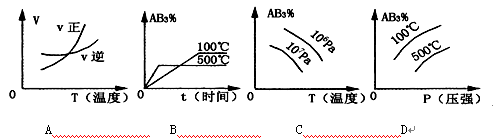
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.是吸热反应 | B.是放热反应 |
| C.是熵减小的反应 | D.是熵增效应大于热效应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
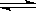 2SO3,当生成2 mol SO3时放出热量为Q,
2SO3,当生成2 mol SO3时放出热量为Q,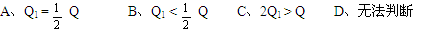
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.低温下为自发过程,高温下为非自发过程 |
| B.高温下为自发过程,低温下为非自发过程 |
| C.任何温度下为非自发过程 |
| D.任何温度下为自发过程 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
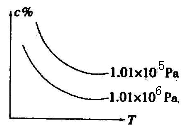
 2Z(g) 现将X和Y以1︰2的体积比混合在密闭容器中,加压到3×107Pa,达到平衡后,已知平衡状态时反应物的总物质的量和生成物的总物质的量相等时,对应图中坐标上的温度是( )
2Z(g) 现将X和Y以1︰2的体积比混合在密闭容器中,加压到3×107Pa,达到平衡后,已知平衡状态时反应物的总物质的量和生成物的总物质的量相等时,对应图中坐标上的温度是( )
| A.100℃ |
| B.200℃ |
| C.300℃ |
| D.不能确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com