
| A.m/55 mol | B.m/87 mol | C.n/11.2 mol | D.n/22.4 mol |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.在CCl4中的溶解性BrCl<Br2 |
| B.BrCl氧化性比Br2强,比Cl2弱 |
| C.沸点BrCl>Br2 |
| D.常温下BrCl可与NaOH溶液反应生成NaCl和NaBrO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 试液.
试液.
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
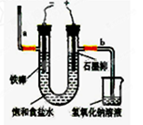

 ,若在标准状态下收集到22.4升的氯气,则被氧化的HCl的物质的量是 。
,若在标准状态下收集到22.4升的氯气,则被氧化的HCl的物质的量是 。 2,为避免此副反应的发生,可采取的措施是 。
2,为避免此副反应的发生,可采取的措施是 。| A.食盐 | B.食醋 | C.烧碱 | D.纯碱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯气可用于杀菌和消毒,这是因为氯气有毒,可毒死病菌 |
| B.干燥的氯气和氯水均能使鲜花褪色 |
| C.漂白粉在空气中容易失效的原因是次氯酸钙不稳定,易分解 |
| D.氢气和氯气的混合气光照生成氯化氢,据此可用于生产盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com