
| A、大于50% |
| B、小于50% |
| C、小于或等于50% |
| D、大于或等于50% |
| a%xg+(100-a)%yg |
| xg+yg |
| (100-2a)%y |
| x+y |
| 1 | ||
1+
|
| 1 | ||
1+
|
| 1 | ||
1+
|
| 1 | ||
1+
|
| 1 |
| 2 |
| 1 | ||
1+
|
| 1 | ||
1+
|
| 1 |
| 2 |
| 1 | ||
1+
|
| 1 |
| 2 |
| 1 | ||
1+
|
| 1 |
| 2 |
| a%xg+(100-a)%yg |
| xg+yg |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ |
| C、③④⑤ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、状态A时I2的转化率比状态B的小 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,一定有v正>v逆 |
| D、状态A与状态B相比,状态A的c(I2)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 被提纯物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 乙酸乙酯(乙酸) | 乙醇 | 蒸馏 |
| C | KNO3(NaCl) | 水 | 降温结晶过滤 |
| D | NaHCO3(溶液)(Na2CO3) | 盐酸 | - |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
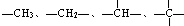 上的碳原子分别称为伯碳、仲碳、叔碳、季碳原子,数目分别用n1、n2、n3、n4表示.例如:2,3,4,4-四甲基己烷.即:
上的碳原子分别称为伯碳、仲碳、叔碳、季碳原子,数目分别用n1、n2、n3、n4表示.例如:2,3,4,4-四甲基己烷.即: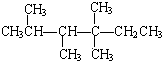 中n1=6,n2=1,n3=2,n4=1.根据不同烷烃的组成和结构,可分析出烷烃(除CH4外)中各原子数的关系.
中n1=6,n2=1,n3=2,n4=1.根据不同烷烃的组成和结构,可分析出烷烃(除CH4外)中各原子数的关系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com