
【题目】由A、D、E、G四种微粒组成的复盐W的化学式为xAaDdyE2DzG.4.704g W溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g.同质量的W与5.13g氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 0.624g,加热后的残渣用水充分溶解后过滤,滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,滴定完毕后,溶液中检测不出任何金属离子和酸根离子;滤渣用硝酸洗涤时部分溶解,得一遇石炭酸显紫色的黄色溶液,依据推理和计算判断:
(1)依次写出D、E、G三种微粒符号、、;
(2)a、d的比值为;
(3)复盐的化学式为 . (写出计算步骤)
【答案】
(1)SO42﹣;NH4+;H2O
(2)1:1
(3)FeSO4?(NH4)2SO4?6H2O
【解析】解:该盐和氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 , 可以证明盐中含有铵根离子,滤渣用硝酸洗涤时部分溶解,得一遇石炭酸显紫色的黄色溶液,即氯化铁溶液,盐中含有铁元素,滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,则复盐W消耗氢氧化钡的物质的量是: ![]() ﹣0.400mol/L×0.015L=0.03mol﹣0.006mol=0.024mol,用H2SO4滴定完毕后,溶液中检测不出任何金属离子和酸根离子,则一定含有SO42﹣ , 根据Ba2++SO42﹣=BaSO4↓,所以含有硫酸根离子的物质的量是0.024mol,W与氢氧化钡充分混匀后加热,生成的气体被足量铝盐溶液分吸收得Al(OH)3 0.624g即0.008mol,3H4+~3NH3H2O~Al(OH),则含有铵根离子的物质的量是0.024mol,4.704gW溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g,则含有水的质量是4.704g﹣3.408g=1.296g,物质的量是0.072mol,所以该盐中
﹣0.400mol/L×0.015L=0.03mol﹣0.006mol=0.024mol,用H2SO4滴定完毕后,溶液中检测不出任何金属离子和酸根离子,则一定含有SO42﹣ , 根据Ba2++SO42﹣=BaSO4↓,所以含有硫酸根离子的物质的量是0.024mol,W与氢氧化钡充分混匀后加热,生成的气体被足量铝盐溶液分吸收得Al(OH)3 0.624g即0.008mol,3H4+~3NH3H2O~Al(OH),则含有铵根离子的物质的量是0.024mol,4.704gW溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g,则含有水的质量是4.704g﹣3.408g=1.296g,物质的量是0.072mol,所以该盐中
n(SO42﹣)、n(NH4+)、n(H2O)分别是0.024mol、0.024mol、0.072mol,化合价规则,含有亚铁离子,质量是3.408g﹣0.024mol×18g/mol﹣0.024mol×96g/mol=0.672g,物质的量是0.012mol,所以复盐的化学式为FeSO4(NH4)2SO46H2O.
(1.)复盐的化学式为FeSO4(NH4)2SO46H2O,D、E、G三种微粒符号是:SO42﹣、NH4+、H2O,故答案为:SO42﹣、NH4+、H2O;
(2.)盐的化学式为FeSO4(NH4)2SO46H2O,a=d=1,即a:d=1:1,故答案为:1:1;
(3.)滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,则复盐W消耗氢氧化钡的物质的量是: ![]() ﹣0.400mol/L×0.015L=0.03mol﹣0.006mol=0.024mol,根据Ba2++SO42﹣=BaSO4↓,所以含有硫酸根离子的物质的量是0.024mol,W与氢氧化钡充分混匀后加热,生成的气体被足量铝盐溶液分吸收得Al(OH)3 0.624g即0.008mol,3H4+~3NH3H2O~Al(OH),则含有铵根离子的物质的量是0.024mol,4.704gW溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g,则含有水的质量是4.704g﹣3.408g=1.296g,物质的量是0.072mol,所以该盐中n(SO42﹣)、n(NH4+)、n(H2O)分别是0.024mol、0.024mol、0.072mol,化合价规则,含有亚铁离子的质量是3.408g﹣0.024mol×18g/mol﹣0.024mol×96g/mol=0.672g,物质的量是0.012mol,所以复盐的化学式为FeSO4(NH4)2SO46H2O.故答案为:FeSO4(NH4)2SO46H2O.
﹣0.400mol/L×0.015L=0.03mol﹣0.006mol=0.024mol,根据Ba2++SO42﹣=BaSO4↓,所以含有硫酸根离子的物质的量是0.024mol,W与氢氧化钡充分混匀后加热,生成的气体被足量铝盐溶液分吸收得Al(OH)3 0.624g即0.008mol,3H4+~3NH3H2O~Al(OH),则含有铵根离子的物质的量是0.024mol,4.704gW溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g,则含有水的质量是4.704g﹣3.408g=1.296g,物质的量是0.072mol,所以该盐中n(SO42﹣)、n(NH4+)、n(H2O)分别是0.024mol、0.024mol、0.072mol,化合价规则,含有亚铁离子的质量是3.408g﹣0.024mol×18g/mol﹣0.024mol×96g/mol=0.672g,物质的量是0.012mol,所以复盐的化学式为FeSO4(NH4)2SO46H2O.故答案为:FeSO4(NH4)2SO46H2O.
根据该盐和氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 , 可以证明盐中含有铵根离子,滤渣用硝酸洗涤时部分溶解,得一遇石炭酸显紫色的黄色溶液,即氯化铁溶液,滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,则复盐W消耗氢氧化钡的物质的量是: ![]() ﹣0.400mol/L×0.015L=0.03mol﹣0.006mol=0.024mol,W与氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 0.624g,可以计算含有的铵根离子的量的多少,用H2SO4滴定完毕后,溶液中检测不出任何金属离子和酸根离子,则一定含有SO42﹣ , 据此回答判断.
﹣0.400mol/L×0.015L=0.03mol﹣0.006mol=0.024mol,W与氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 0.624g,可以计算含有的铵根离子的量的多少,用H2SO4滴定完毕后,溶液中检测不出任何金属离子和酸根离子,则一定含有SO42﹣ , 据此回答判断.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知2Mg+CO2![]() 2MgO+C,某同学根据金属活动顺序表推测钠与CO2也能反应,为探究反应产物,利用下图装置进行实验。(已知PdCl2能被CO还原为黑色的Pd,饱和NaHCO3溶液可以用于除去CO2 中的HC1气体)
2MgO+C,某同学根据金属活动顺序表推测钠与CO2也能反应,为探究反应产物,利用下图装置进行实验。(已知PdCl2能被CO还原为黑色的Pd,饱和NaHCO3溶液可以用于除去CO2 中的HC1气体)
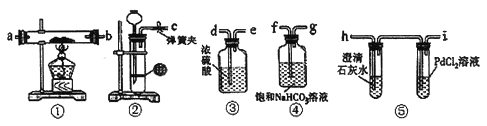
(1)原料中的金属钠通常保存在______中,实验室取用少量金属钠需要用到的实验用品有_____,____,玻璃片和小刀等。
(2)装置②中用稀盐酸与CaCO3反应制备CO2,制备该气体时发生反应的离子方程式是___________。
(3)请将图中各装置按顺序连接(填裝置接口字母): c接____,____接____,____接____,_____接______。
(4)装置③的作用是___________。
(5)检查完装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到________时再点燃酒精灯。此步操作的目的是__________。
(6)根据下列实验现象,推测并请写出钠与CO2反应的化学方程式___________。
I.实验过程中若观察到装置⑤PdCl2溶液中有黑色沉淀,且装置①中固体成分只有一种,向固体中加入稀盐酸可产生能使澄清石灰水变浑独的气体。请写出钠与CO2反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应:C(s)+ ![]() O2(g)═CO(g)△H1<0,CO(g)+
O2(g)═CO(g)△H1<0,CO(g)+ ![]() O2(g)═CO2(g)△H2<0, C(s)+O2(g)═CO2(g)△H3<0;下列说法正确的是( )
O2(g)═CO2(g)△H2<0, C(s)+O2(g)═CO2(g)△H3<0;下列说法正确的是( )
A.56 g CO和32 g O2所具有的总能量小于88 g CO2所具有的总能量
B.碳的燃烧热是△H3
C.△H1<△H3
D.28 g CO的总能量比44 g CO2的总能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从有机物A开始有如图所示的转化关系(部分产物略去).A在NaOH溶液中水解生成B、C和D,1molF与足量的新制Cu(OH)2碱性悬浊液加热充分反应可生成2mol红色沉淀.分析并回答问题: 
(1)A中含有的官能团为氯原子(﹣Cl)和、;
(2)指出反应类型:A→B、C、D; H→I;
(3)写出下列反应的化学方程式:
①C→F:;②E→H:;
(4)与E含有相同官能团的某有机物甲(C4H8O3)有多种同分异构体,在结构中含有酯基和羟基,且水解产物不存在两个羟基连在同一个碳上的同分异构体有种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气, ![]() 减小
减小
B.通入少量SO2 , 溶液的漂白性增强
C.加入少量水,水的电离平衡向正反应方向移动
D.加入少量固体NaOH,一定有c(Na+)=c(Cl﹣)+c(ClO﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的两个电化学装置,图1中铜电极上产生大量的无色气泡;图2中铜电极上无气体产生,而铬电极上产生大量的有色气体.根据上述现象判断下列说法不正确的是( ) 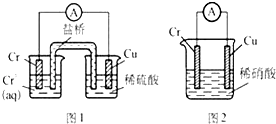
A.图1中Cr为正极,Cu为负极
B.图2中Cu电极上发生的离子方程式为:Cu﹣2e﹣═Cu2+
C.金属铬的活泼性比铜强且能和硫酸反应生成H2
D.金属铬易被稀硝酸钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体体积的大小与许多因素有关.当温度和压强相同时,气体体积主要取决于
A.气体的物质的量 B.气体分子之间的平均距离
C.气体分子本身的大小 D.气体的种类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com