
| 实验步骤 | 实验现象 | 实验结论和解释 |
| 取少量上述无色溶液于试 管中,逐滴加入NaOH溶液,直至过量,再加热 | 生成白色沉淀, ______ ______ | 无色溶液中存在Zn2+、NH4+离子 检验NH4+离子存在的离子方程式是 ______ |
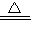 NH3↑+H2O,产生有刺激性气味的气体,故答案为:白色沉淀消失,产生有刺激性气味的气体;NH4++OH-
NH3↑+H2O,产生有刺激性气味的气体,故答案为:白色沉淀消失,产生有刺激性气味的气体;NH4++OH-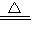 NH3↑+H2O;
NH3↑+H2O;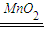 2H2O+O2↑,生成56ml氧气,即
2H2O+O2↑,生成56ml氧气,即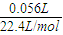 =0.0025mol,则消耗的H2O2物质的量为0.005mol,
=0.0025mol,则消耗的H2O2物质的量为0.005mol,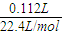 =0.005mol,则消耗的H2O2物质的量为0.005mol,故答案为:1:1;H2O2+2H++MnO2=Mn2++2H2O+O2↑.
=0.005mol,则消耗的H2O2物质的量为0.005mol,故答案为:1:1;H2O2+2H++MnO2=Mn2++2H2O+O2↑.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解

| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量上述无色溶液于试管中,逐滴加入NaOH溶液,直至过量. | 生成白色沉淀, 白色沉淀逐渐溶解,产生刺激性气味的气体 白色沉淀逐渐溶解,产生刺激性气味的气体 |
无色溶液中 存在Zn2+离子 |
| ② 将溶液加热,并将湿润的红色石蕊试纸贴在玻璃棒的一端置于试管口 将溶液加热,并将湿润的红色石蕊试纸贴在玻璃棒的一端置于试管口 |
红色石蕊试纸变蓝 红色石蕊试纸变蓝 |
无色溶液中 存在NH4+离子 |
| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论与解释 |
| 实验一 | 足量MnO2 | 收集到56mL气体 | MnO2做催化剂 |
| 实验二 | 足量MnO2 和稀硫酸 |
黑色粉末部分溶解, 收集到112mL气体 |
MnO2做氧化剂 MnO2做氧化剂 生成Mn2+离子 生成Mn2+离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
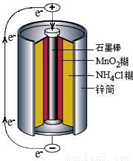
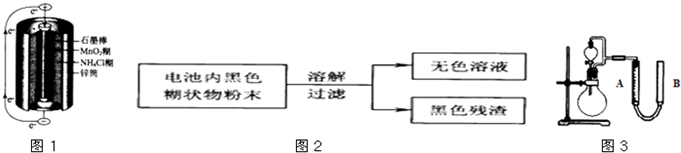
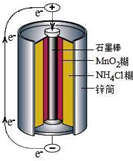
 锌锰干电池是最早使用的化学电池,其基本构造如图所示.
锌锰干电池是最早使用的化学电池,其基本构造如图所示.| 实验步骤 | 实验现象 | 实验结论和解释 | ||||||||
| 取少量上述无色溶液于试 管中,逐滴加入NaOH溶液,直至过量,再加热 | 生成白色沉淀, 白色沉淀消失, 白色沉淀消失, 产生有刺激性气味的气体 产生有刺激性气味的气体 |
无色溶液中存在Zn2+、NH4+离子 检验NH4+离子存在的离子方程式是 NH4++OH-
NH4++OH-
|

| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论与解释 |
| 实验一 | 足量MnO2 | 收集到56mL气体 | MnO2做催化剂 |
| 实验二 | 足量MnO2和稀硫酸 | 黑色粉末部分溶解, 收集到112mL气体 |
MnO2做氧化剂,生成Mn2+离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量上述无色溶液于试管中,逐滴加入NaOH溶液,直至过量. | 生成白色沉淀,______ | 无色溶液中 存在Zn2+离子 |
| ②______ | ______ | 无色溶液中 存在NH4+离子 |
| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论与解释 |
| 实验一 | 足量MnO2 | 收集到56mL气体 | MnO2做催化剂 |
| 实验二 | 足量MnO2 和稀硫酸 | 黑色粉末部分溶解, 收集到112mL气体 | ______ ______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验步骤 | 实验现象 | 实验结论和解释 |
| 取少量上述无色溶液于试 管中,逐滴加入NaOH溶液,直至过量,再加热 | 生成白色沉淀, ______ ______ |
无色溶液中存在Zn2+、NH4+离子 检验NH4+离子存在的离子方程式是 ______ |
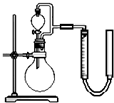
| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论与解释 |
| 实验一 | 足量MnO2 | 收集到56mL气体 | MnO2做催化剂 |
| 实验二 | 足量MnO2和稀硫酸 | 黑色粉末部分溶解, 收集到112mL气体 |
MnO2做氧化剂,生成Mn2+离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com