
【题目】浓硫酸滴在滤纸上,滤纸变黑,表明浓硫酸具有( )
A.脱水性B.吸水性C.酸性D.不挥发性
科目:高中化学 来源: 题型:
【题目】某兴趣小组甲设计了以下装置和方法测定空气中SO2含量.你认为可行的操作是
序号 | A | B | C |
装置 |
|
|
|
原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50 mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的是验证:同一主族,从上到下金属元素的原子失电子能力逐渐增强;同一周期,从左到右金属元素的原子失电子能力逐渐___________________;
(2)反应最剧烈的烧杯中金属是_______(填字母序号);
A.钠 B.镁 C.铝 D.钾
(3)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法_________(填字母序号)。
A.把镁、铝的金属块换成金属粉末
B.把烧杯中的冷水换成热水
C.把烧杯中的冷水换成盐酸
D.把烧杯中的冷水换成氢氧化钠溶液
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题
(1)实验装置:

(1)填写所示仪器名称:B__________
(2)实验步骤:
连接仪器、_____________、加药品后,打开 a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是________________________________;装置E中酸性KMnO4溶液的作用是_____________________________;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是__________________;试管F中发生反应的离子方程式为_____________________。
③依据试管 D 中的反应,能否证明S的非金属性强于C的非金属性___(填 “能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不正确的是
A. 化学的特征就是认识分子和制造分子,它是一门具有创造性和实用性的科学
B. 人们可以利用先进的化学技术制造出新的原子和新的分子
C. 制陶、酿酒过程中,肯定发生了化学变化
D. 化学家可以在微观层面上操纵分子和原子,组装分子器件和分子机器等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃与氢气发生反应后能生成(CH3)2CHCH2CH3 , 则该烃不可能是( )
A.2﹣甲基﹣2﹣丁烯
B.3﹣甲基﹣1﹣丁烯
C.2,3﹣二甲基﹣1﹣丁烯
D.2﹣甲基﹣1,3﹣丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是 
(1)电源B极是极(填“正”或“负”)
(2)(甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量比为 .
(3)欲用(丙)装置给钢镀银,G应该是(填电极材料),电镀液选溶液.
(4)电解一段时间后,加入何种物质能使溶液恢复到原来浓度,甲应加入乙应加入 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是典型的可充电电池,正负极是惰性材料,电池总反应式为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,回答下列问题(不考虑氢、氧的氧化还原):
2PbSO4+2H2O,回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时,正极的电极反应式是________________。当外电路通过2 mol电子时,理论上负极板的质量增加______,电池中消耗硫酸物质的量为______。
(2)在完全放电耗尽PbO2和Pb时,若按下图连接,电解一段时间后,则在A电极上生成____________,此时铅蓄电池的正负极的极性将___________。(填“不变”或“对换”)

(3)若用铅蓄电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=0.3 mol·L-1,取该混合液100 mL,用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112 L(标准状况)气体,则铅蓄电池中转移电子的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(s)+n D(g)pX(g)+qY(g)在反应过程中,其他条件不变,D的转化率和温度T 或压强P关系如图所示(D%为D的转化率),下列叙述中正确的是( ) 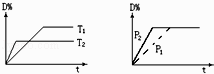
A.正反应为放热反应
B.使用催化剂,D的物质的量减小
C.化学方程式系数m+n=p+q
D.增加物质A或D的用量,平衡均向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知图一表示的是可逆反应CO(g)+H2(g)C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( ) 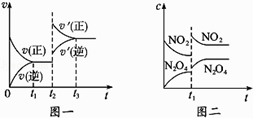
A.图一t2时改变的条件可能是升高了温度或增大了压强
B.图一t2时改变的条件是增大压强,则反应的△H增大
C.图二t1时改变的条件可能是升高了温度
D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com