
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )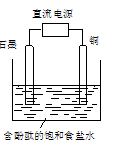
| A.铜电极附近观察到黄绿色气体 |
| B.石墨电极附近溶液呈红色 |
| C.溶液中的Na+向石墨电极移动 |
| D.铜电极上发生还原反应 |
科目:高中化学 来源: 题型:单选题
如图为氢氧燃料电池原理示意图,下列叙述不正确的是
| A.a电极是负极 |
| B.b电极上发生氧化反应 |
| C.该电池工作时化学能转化为电能 |
| D.该电池的总反应为2H2 + O2 = 2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3—)=6.0 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
| A.原混合溶液中n(K+)为2 mol |
| B.上述电解过程中共转移4 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol |
| D.电解后溶液中c(OH—)为2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图所示装置I是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为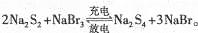 闭合开关K时,b极附近先变红色。下列说法正确的是
闭合开关K时,b极附近先变红色。下列说法正确的是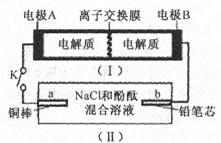
| A.当有0.01 mol Na+通过离子交换膜时,b电极上析出112 mL的气体 |
| B.负极反应为3Br--2e-= Br3- |
| C.闭合K后,b电极附近的pH变小 |
| D.闭合K后.a电极上有氯气产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔融)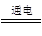 4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH
4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH 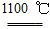 Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
| A.电解熔融氢氧化钠制钠,阳极发生的电极反应为2OH--2e-=H2↑+O2↑ |
| B.若用戴维法与吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| C.吕萨克法制钠的原理是利用铁的还原性比钠强 |
| D.目前工业上常用电解熔融氯化钠法制钠(如下图),电解槽中石墨为阳极,铁为阴极 |
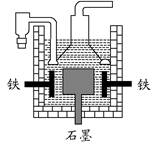
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑点向d端扩散。下列判断正确的是( )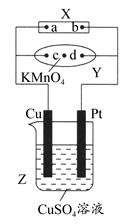
| A.滤纸上c点附近会变红色 |
| B.Cu电极质量减小,Pt电极质量增大 |
| C.Z中溶液的pH先减小,后增大 |
| D.溶液中的SO42—向Cu电极定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关电化学知识的描述正确的是 ( )
| A.CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3=Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
钢铁生锈过程发生如下反应:①2Fe+O2+2H2O=2Fe(OH)2;②4Fe(OH)2+O2+2H2O=4Fe(OH)3;③2Fe(OH)3=Fe2O3+3H2O。下列说法正确的是( )。
| A.钢铁在碱性条件下腐蚀生成铁锈,而在酸性条件下不生成铁锈 |
| B.反应①中的氧化剂是氧气和水 |
| C.上述反应表示钢铁发生的是吸氧腐蚀 |
| D.钢铁在潮湿的空气中不能发生电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存相同的一段时间。下列对实验结束时现象的描述不正确的是 ( )。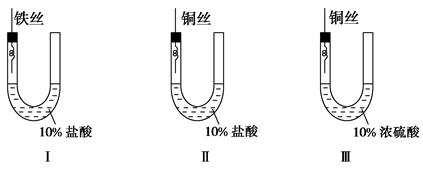
| A.装置Ⅰ左侧的液面一定会下降 |
| B.左侧液面装置Ⅰ比装置Ⅱ的低 |
| C.装置Ⅱ中的铁钉腐蚀最严重 |
| D.装置Ⅲ中的铁钉几乎没被腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com