
标准状况下,将3.36 L CO2气体通入200 mL 1.00 mol·L-1 NaOH溶液中,充分反应后溶液中c(CO )与 c(HCO
)与 c(HCO )的比值为(不考虑CO
)的比值为(不考虑CO 、HCO
、HCO 的水解) ( )
的水解) ( )
A.1∶1 B.1∶2
C.2∶1 D.1∶3
科目:高中化学 来源: 题型:
下列有关实验的描述正确的是
A.用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈酸性
B.中和滴定实验中,锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,须干燥 或用待装液润洗后方可使用
C.将碘水倒入分液漏斗,加入适量乙醇,振荡后静置,能将碘萃取到乙醇中
D.向含有FeCl2杂质的FeCl3溶液中通入足量C12后,充分加热蒸干,可得到纯净的FeCl3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的装置,在盛有水的烧杯中,铁圈和银圈的相接处吊着一根绝缘的细丝,使之平衡。小心地从烧杯中央滴入AgNO3溶液。片刻后可观察到的现象是(指悬吊的金属圈)
 A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
查看答案和解析>>
科目:高中化学 来源: 题型:
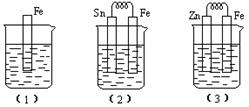
如下图所示,烧杯中都盛有稀硫酸:
① 装置(2)中Fe电极的电极反应:
,
装置(3)中Fe电极的电极反应:
;
② 装置(2)Sn极附近溶液的pH ;(填:“增大”、“减小”或“不变”)
③ 比较(1)、(2)、(3)中铁被腐蚀的速率由快到慢的顺序是 。(填“序号”)
查看答案和解析>>
科目:高中化学 来源: 题型:
写出除去下列气体中混有的杂质(括号内为杂质)可采取的方法:
(1)CO(CO2):__________________________________________________________。
(2)CO2(CO):__________________________________________________________。
(3)CO2(O2):__________________________________________________________。
(4)CO2(SO2):_________________________________________________________。
(5)CO2(HCl):_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
ⅰ.高温下用碳还原二氧化硅制得粗硅
ⅱ.粗硅与干燥HCl气体反应制得SiHCl3:
Si+3HCl SiHCl3+H2
SiHCl3+H2
ⅲ.SiHCl3与过量H2在1 000~1 100 ℃反应制得纯硅
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第ⅰ步制备粗硅的化学反应方程式为___________________________________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量SiCl4(沸点
57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3采用的方法为______________________。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①装置B中的试剂是____________________________________________________。
装置C中的烧瓶需要加热,其目的是__________________________________ _____。
_____。
②反应一段时间后,装置D中观察到的现象是_______________________________,
装置D不能采用普通玻璃管的原因是_______________________________________,
装置D中发生反应的化学方程式为_________________________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及__________________。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂是______(填写字母代号)。
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液
e.Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于SiO2和CO2的叙述中不正确的是 ( )
A.都是共价化合物
B.都是酸性氧化物,都能与强碱溶液反应
C.都能溶于水且与水反应生成相应的酸
D.SiO2可用于制光导纤维,干冰可用于人工降雨
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Mg2+、Al3+等离子。当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如下图所示。由此可知原溶液中
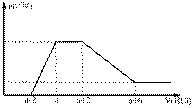 A.不含SO42-
A.不含SO42-
B.含有的阴离子一定是OH-、AlO2-、SiO32-
C.含有的阴离子一定是OH-、CO32-、AlO2-、SiO32-
D.含有AlO2-与SiO32-的物质的量之比为3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com