
��16�֣� ��ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ�á�
��1�����á���ѧ����ת�Ʒ����ᴿ�����ٵķ�Ӧԭ��ΪW(s)��I2(g) WI2(g)���÷�Ӧ��ʯӢ��չ��н��У�����ͼ��ʾ��
WI2(g)���÷�Ӧ��ʯӢ��չ��н��У�����ͼ��ʾ��
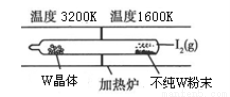
�ٸ÷�Ӧ��ƽ�ⳣ������ʽK��_______����K��1/2����ij�����ܱ������м���1mol I2(g)������W(s)����Ӧ�ﵽƽ��ʱI2(g)��ת����Ϊ__________��
�ڸ÷�Ӧ�ġ�H____0���������������������Ӧ��ϵ�п�ѭ��ʹ�õ�����____��
���ܹ�˵��������Ӧ�Ѿ��ﵽƽ��״̬����_________������ţ���
a��I2��WI2��Ũ�����
b��W���������ٱ仯
c�������ڻ��������ܶȱ��ֲ���
d����λʱ���ڣ����������ĵ����ʵ�����⻯�����ɵ����ʵ������
��2�����á���Ĥ��ⷨ��������Ũ����ȩ��ˮ�Ĺ��վ������̼��ܺĽϵ͵��ŵ㣬��ԭ����ʹ��ȩ�ֱ�����������������Ӧ�����Ҵ������ᣬ�ܷ�ӦʽΪ2CH3CHO��H2O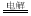 CH3CH2OH��CH3COOH��ʵ�����У���һ��Ũ�ȵ���ȩ��Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ��
CH3CH2OH��CH3COOH��ʵ�����У���һ��Ũ�ȵ���ȩ��Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ��
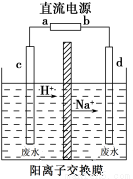
�����Լ������ȼ�ϵ��Ϊֱ����Դ����ȼ�ϵ����b��Ӧͨ��__________(�ѧʽ)��
�ڵ����������ĵ缫��ӦʽΪ_________________��
����ʵ�ʹ��մ����У���������ȩ��ȥ���ʿɴ�60%�������������ֱ�ע��1 m3��ȩ����Ϊ3000 mg��L-1�ķ�ˮ���ɵõ��Ҵ�________kg(����������С�����һλ)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и���ѧҵˮƽģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʣ����������ᷴӦ����������������Һ��Ӧ����
A��AlCl3 B��Al(OH)3 C��KOH D��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫�߿���ɽ�и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������װ��˵����ȷ����

A��װ�â��е�ͭ����ð����
B����a��b����ʯī��װ�â��е�a��b ð����
C��װ�âٻ�������ͭ��Һ����ʵ��пƬ�϶�ͭ
D��װ�âڻ�������ͭ��Һ����ʵ�֡�b������ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�ɶ��и���4��ģ�⿼���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A��Na������O2��ȼ�գ�����lmol O2ʱת�Ƶĵ�������4��6.02��1023
B������ʹ���Ļ����ҺpH=1������Һ��c(H+) = 0.1 mol/L
C��1 L 0.1 mol/L NH4Cl��Һ�е�N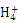 ����0.1��6.02��1023
����0.1��6.02��1023
D����״����2.24 L Cl2�к���0.2 mol ���ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�ɶ��е�������ϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ��װ����Ʋ�ǡ������
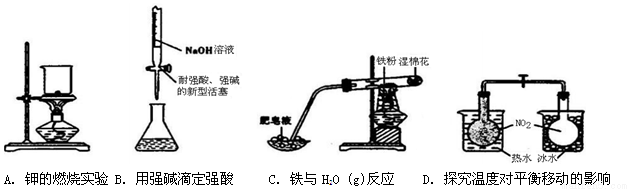
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и�����ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����10 mL 0.1 mol��L-1��NH3��H2O��Һ������˵����ȷ����
A��25��ʱ������Һ��pH=11����Kb(NH3��H2O)=1��10-6
B������Һ�м�������CH3COONa���壬��Һ�� ��ֵ��С
��ֵ��С
C������Һ�м���10 mL 0.1 mol��L-1���ᣬ������Һ������Ũ�ȴ�С˳��Ϊ��c(NH4+)��(Cl-)��c(H+)��c(OH-)
D������Һ�м���5 mL 0.1 mol��L-1���ᣬ������Һ�����ӵ�Ũ��һ�����ϣ�c(NH4+) + c(H+) = c(Cl-) + c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и�����ѧ�ڶ�ģ�������ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
(���14��)ij��(H)��һ�ֺϳɶ��������м��壬��������·�ߺϳ�(���ַ�Ӧ������ȥ)��
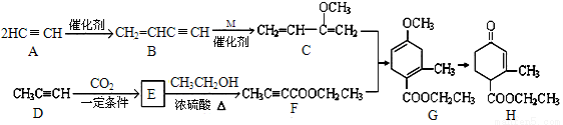
��1��A��B�ķ�Ӧ������ ��B��CΪ�ӳɷ�Ӧ������M�Ľṹ��ʽ�� ��
��2��H�г����ʻ�(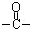 )�⣬���еĹ����������� ��
)�⣬���еĹ����������� ��
��3��ʵ������A�Ļ�ѧ����ʽΪ ��
��4��E�� F�Ļ�ѧ����ʽ�� ��
��5������˵����ȷ���� ��
a. D��F�о�����Ȳ��������
b. A�ܺ�HCl��Ӧ�õ�������ϩ�ĵ���
c. 1mol G��ȫȼ������7mol H2O
d. H�ܷ����ӳɡ�ȡ����Ӧ
��6��TMOB��H��ͬ���칹�壬�������нṹ�������ٺ˴Ź������ױ����������г������⣬������ԭ�ӻ�ѧ������ͬ���ڴ��ڼ�����(CH3O-)��TMOB�Ľṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������и������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A����֪����ƽ�ⳣ����H2CO3��HClO��HCO3������NaClO��Һ��ͨ������CO2��2ClO��+CO2+H2O��2HClO+CO32��
B��������������Һ�еμ�Ba(OH)2�����ԣ�H++SO42-+Ba2++ OH-��BaSO4��+ H2O
C��Fe(NO3)3��Һ�м��������HI��Һ��2Fe3�� + 2I����2Fe2�� + I2
D����������ӵĵ��뷽��ʽ��HS����H2O H3O����S2��[
H3O����S2��[
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����4�¹����Լ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
(17��)���û�ѧ��Ӧԭ���о�̼��������Ԫ�ؼ��仯��������Ҫ���塣
��1����֪һ������C��������O2(g)��ȼ�գ�����ܵIJ��P������ϵ��ͼ��ʾ��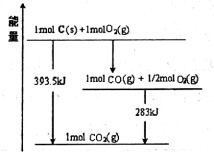
д��CO2(g)��C(s)��Ӧ����CO(g)���Ȼ�ѧ����ʽ_______________________��
��2������β�����������з�����Ӧ2NO(g)+2CO(g) N2+2CO2(g) ��H<0��һ�������£���ij�ܱպ��������а������1��l����44.8L(��״��)NO��CO������壬����������Ӧ��ijͬѧ���ݷ�Ӧ�����е��й����ݻ�������ͼ��ʾ���ߡ�
N2+2CO2(g) ��H<0��һ�������£���ij�ܱպ��������а������1��l����44.8L(��״��)NO��CO������壬����������Ӧ��ijͬѧ���ݷ�Ӧ�����е��й����ݻ�������ͼ��ʾ���ߡ�
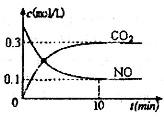
�����й���������Ӧ���̵�������ȷ���� ________(��д��ĸ����)��
A�������������䣬�����������H��ֵ����
B����ʱ��ȥ������̼����Ӧ������Ӧ���ʼӿ�
C��NO��CO��N2��CO2Ũ�Ⱦ����ٱ仯��˵��ƽ��δ�����ƶ�
D����������ƽ����Է����������ٸı䣬֤����Ӧ�ﵽ��ѧƽ��״̬
��ǰ10min��CO��ƽ����Ӧ����Ϊ______����ƽ��ʱNO��ת����Ϊ_____����ʹ����ƽ����ϵ��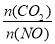 ����Ĵ�ʩ��__________(��дһ��)��
����Ĵ�ʩ��__________(��дһ��)��
��3����֪���������ˮ�еĵ���ƽ�ⳣ��(25��)���±�(��λʡ��)��
������� | H2CO3 | H2SO3 | NH3��H2O |
����ƽ�ⳣ�� | Ka1=4.2��10��7 Ka2=5.6��10��11 | Ka1=1.54��10��2 Ka2=1.02��10��7 | Kb=1.7��10��5 |
�����������¡��ó����������Ȱ�ˮһ��ʱ�䣬�ָ������º���Һ��ˮ�ĵ���̶ȱȼ���ǰ_______(��д����������С�����䡱)�ˣ�
�ڳ����£�0.1 mo1��L-1(NH4)2SO4��Һ��_____(��ᡱ�����С������)�ԡ�
�۳����£����ij̼�����ϵ�pH=6���������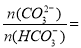 ________��
________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com