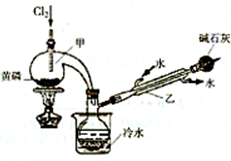
某化学实验兴趣小组为探究实验室制备Cl
2 的过程中有水蒸气和HCl挥发来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略):

试回答下列问题:
(1)下列方法中,可制得氯气的是
①②③④⑤
①②③④⑤
.
①MnO
2和浓盐酸混合共热 ②MnO
2、NaCl和浓硫酸混合共热③次氯酸钠和浓盐酸混合 ④KClO
3和浓盐酸混合共热
⑤KMnO
4和浓盐酸混合
(2)若用含有0.2mol HCl 的浓盐酸与足量MnO
2反应制取Cl
2,制得的Cl
2在标准状况下的体积总是小于1.12L的原因是
浓盐酸的浓度随反应的不断进行逐渐变稀,变稀后将不再反应
浓盐酸的浓度随反应的不断进行逐渐变稀,变稀后将不再反应
.
(3)①装置B的作用是
证明有水蒸气产生
证明有水蒸气产生
,现象是
白色固体变蓝色
白色固体变蓝色
.②装置C和D出现的不同现象说明的问题是
氯气无漂白性,次氯酸有漂白性
氯气无漂白性,次氯酸有漂白性
.
③装置E 的作用应该是
吸收氯气
吸收氯气
.④写出装置F中发生反应的离子方程式
Ag++Cl-=AgCl↓
Ag++Cl-=AgCl↓
.
(4)乙同学认为甲同学的实验有缺陷,不能确认最终通入AgNO
3溶液中的气体只有一种,为了保证实验结论的可靠性,证明最终通入AgNO
3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置.你认为该装置应加在
E与F
E与F
之间(填装置字母序号),装置中应加入
碘化钾淀粉试液
碘化钾淀粉试液
.



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案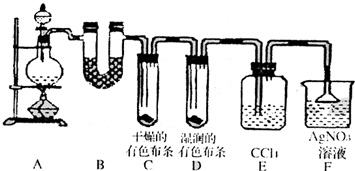 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.