
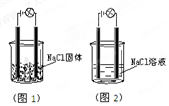
 一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl是非电解质 | B. | NaCl溶液是电解质 | ||
| C. | NaCl在水溶液中离子键发生断裂 | D. | NaCl溶液中水电离出大量的离子 |
分析 根据原电池的工作原理和构成条件:电解质溶液必须含有大量自由移动离子,电解质中阴阳离子的定向移动形成电流,在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液和熔融状态下都不导电的化合物是非电解质,含有自由移动的离子或电子的物质能导电,据此分析解答.
解答 解:A.NaCl晶体中不含自由移动的阴阳离子或电子,所以不导电,但NaCl在熔融状态下能导电,所以属于电解质,故A错误;
B.氯化钠溶液含有自由移动的离子,所以能得电子,但NaCl溶液是混合物,既不是电解质也不是非电解质,故B错误;
C.NaCl在水溶液中离子键发生断裂,电离出了可以自由移动的离子,所以NaCl溶液能导电,故C正确;
D.氯化钠固体中的钠离子和氯离子不能自由移动,在水分子的作用下电离出阴阳离子,故D错误;
故选C.
点评 本题考查电解质、非电解质的判断,侧重考查对概念的理解,注意概念中的关键词,注意二者的区别,注意:单质和混合物既不是电解质也不是非电解质,为易错点,题目难度不大.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | ③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶内的液面以下 | |
| C. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
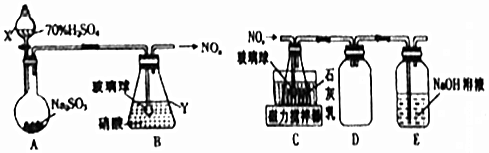
 磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答:
磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷跟氯气发生取代反应 | B. | 乙烯跟氯气发生加成反应 | ||
| C. | 乙烷跟氯化氢混合 | D. | 乙烯跟氯化氢发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com