
【题目】在蛋白质溶液中分别进行下列操作或加入下列物质,其中一种与其它三种现象有本质不同的是
A.加硫酸铵的浓溶液 B.加浓硝酸 C.加热 D.加硫酸铜溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】I. ![]() U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。![]() U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:
(1)![]() U表示的含义是________________。
U表示的含义是________________。
(2)![]() U、
U、![]() U、
U、![]() 互为同位素,下列对同位素的理解不正确的是________(填序号,下同)。
互为同位素,下列对同位素的理解不正确的是________(填序号,下同)。
A.元素符号相同 B.物理性质相同
C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关![]() U说法不正确的是________。
U说法不正确的是________。
A.![]() U原子核的中子数与质子数之差为51
U原子核的中子数与质子数之差为51
B.![]() U与
U与![]() U的质子数、电子数都相等
U的质子数、电子数都相等
C.![]() U与
U与![]() U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子
D.![]() U与
U与![]() U是同种原子
U是同种原子
Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)Li和Li作核反应堆最佳载热体,LiH和LiD作高温堆减速剂。下列说法中 正确的是________(填序号,下同)。
A.Li和Li互为同位素 B.Li和Li属于同种核素
C.LiH和LiD的化学性质不同 D.LiH和LiD是同种物质
(2)下列说法不正确的是________。
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
(3)锂是碱金属族首元素,其性质明显不同于其他碱金属性质,下列能支持这一观点的性质是________。
A.碱金属与水反应 B.碱金属在氧气中燃烧
C.碱金属与氢气反应 D.碱金属与氯气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol H2(g)和2mol I2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+ I2(g) ![]() 2HI(g) △H<0,达平衡,HI的体积分数ω(HI)随时间变化如图Ⅱ所示,若改变反应条件,ω(HI)的变化曲线如图Ⅰ所示,则改变的条件可能是( )
2HI(g) △H<0,达平衡,HI的体积分数ω(HI)随时间变化如图Ⅱ所示,若改变反应条件,ω(HI)的变化曲线如图Ⅰ所示,则改变的条件可能是( )

A.恒温恒容条件下,加入适当催化剂
B.恒温条件下,缩小反应容器体积
C.恒温条件下,扩大反应容器体积
D.恒容条件下升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不正确的是( )
A. 滴定前用待测液润洗锥形瓶
B. 容量瓶和滴定管使用前均需要检漏
C. 蒸馏完毕时,先停止加热,再关闭冷凝水
D. 分液时,下层溶液先从下口放出,上层溶液再从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医用氯化钙可用于生产补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2、2H2O的质量分数为97.0%~103.0%)的主要流程如下:
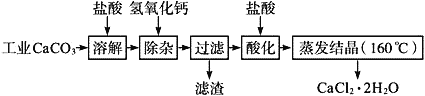
已知:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Al(OH)3 | |
开始沉淀时的pH | 2.3 | 4.0 | 开始溶解时的pH | 7.8 |
完全沉淀时的pH | 3.7 | 5.2 | 完全溶解时的pH | 10.8 |
(1)CaCO3与盐酸反应的离子方程式___________。
(2)“除杂”操作是加入氢氧化钙,调节溶液的pH范围为________,目的是除去溶液中的少量Al3+、Fe2+。
(3)过滤时需用的比玻璃器有__________。
(4)“酸化”操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①防止氢氧化钙吸收空气中的二氧化碳;②防止Ca2+在蒸发时水解;③_______。
(5)蒸发结晶要保持在160℃的原因是__________。
(6)测定样品中Cl-含量的方法是:称取0.750 0 gCaCl2·2H2O样品,溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中;用0.050 00 mol/L AgNO3溶液滴定至终点(用K2Cr2O2),消耗AgNO3溶液体积的平均值为20.39 mL。
①上述测定过程中需用溶液润洗的仪器有________。
②计算上述样品中CaCl2·2H2O的质量分数为_______。(保留四位有效数字)
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有________;__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液含有下列离子中的若干种:H+、NH4+、Fe3+、Ba2+、Al3+、CO32-、Cl-、OH-、NO3-。向该溶液中加入铝粉,只放出H2,则溶液中能大量存在的离子最多有
A. 4 种 B. 5 种 C. 6 种 D. 7 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水中的电离方程式是H2A=H++HA-,HA-![]() H++A2-。回答下列问题:
H++A2-。回答下列问题:
(1) Na2A溶液显 (填“酸性”、“中性”或“碱性”),理由是 (用离子方程式或必要的文字说明)。
(2) 常温下,已知0.1 mol·L-1NaHA溶液pH=2,则0.1 mol·L-1H2A溶液中氢离子的物质的量浓度可能 0.11 mol·L-1(填“大于”、“等于”或“小于”), 理由是 。
(3) 0.1 mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是
(4) Na2A溶液中,下列表述正确的是
A.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
B.c(Na+)=2[c(HA-)+c(A2-)+c(H2A)]
C.c(OH-)=c(HA-)+c(H+)+2c(H2A)
D.c(OH-)=c(HA-)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质熔融状态可导电,固态可导电,将其投入水中溶液也可导电,推测该物质可能是 ( )
A. 金属 B. 非金属 C. 可溶性碱 D. 可溶性盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4CO(g)+2NO2(g)![]() N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol/L,N2的浓度为0,2 min后测得N2的浓度为0.6 mol/L,则此段时间内,下列反应速率表示正确的是
N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol/L,N2的浓度为0,2 min后测得N2的浓度为0.6 mol/L,则此段时间内,下列反应速率表示正确的是
A.v(CO)=1.2 mol/(L·s) B.v(NO2)=0.3 mol/(L·min)
C.v(N2)=0.6 mol/(L·min) D.v(CO2)=1.2 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com