
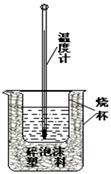
科目:高中化学 来源:不详 题型:实验题
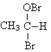
| 实验操作 | 预期现象与结论 |
| 步骤1:取一定量 B 于试管中,然后边震荡试管边慢慢加入适量 C 和 D 。 | |
| 步骤2:固定好装置,用酒精灯缓慢加热。将产生的蒸气通到 E 溶液的液面上。 | F , G 。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
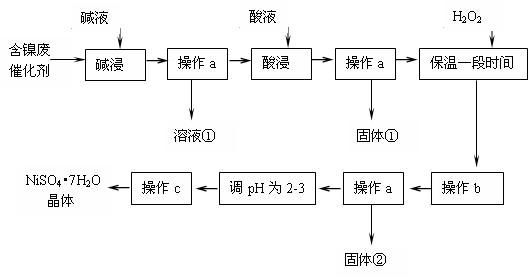
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
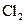 、
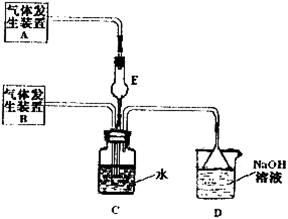
、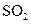 气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸为原料制取C12。在此实验中,E仪器的作用是__________;发生装置B应选择以下三种装置中的___________(填序号)。
气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸为原料制取C12。在此实验中,E仪器的作用是__________;发生装置B应选择以下三种装置中的___________(填序号)。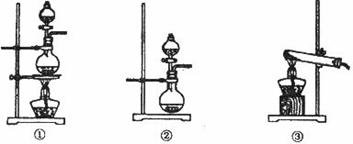
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器。
和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器。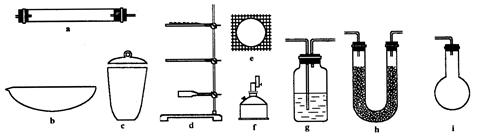
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
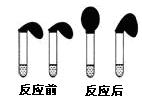
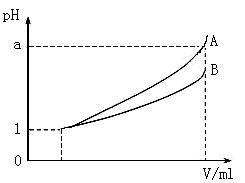
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3COOH+Cu2O↓+2H2O”提出了质疑,并进行如下探究:
CH3COOH+Cu2O↓+2H2O”提出了质疑,并进行如下探究: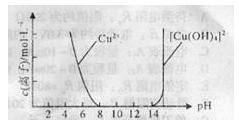
 CH3COOH+Cu2O↓+2H2O”质疑的理由:
CH3COOH+Cu2O↓+2H2O”质疑的理由:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
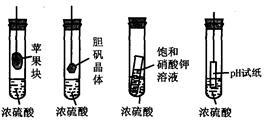
| A.苹果块会干瘪 | B.胆矾晶体表面有“白斑” |
| C.小试管内有晶体析出 | D.pH试纸变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实 验 事 实 | 结 论 |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| D | SO2通入KMnO4溶液,溶液褪色 | SO2具有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com