
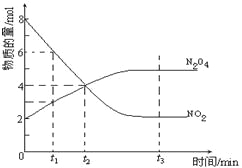
【题目】一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: molL﹣1s﹣1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 (填“>”、“<”或“=”)逆反应速率.
【答案】(1)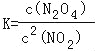 ;
;
(2)0.1;
(3)t3;
(4)>.
【解析】
试题分析:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;
(2)由图可知,从t1至t2时N2O4的物质的量变化量为4mol﹣3mol=1mol,根据v=![]() 计算v(N2O4);
计算v(N2O4);
(3)到达平衡时,反应混合物各组分的物质的量不发生变化,据此结合图象判断;
(4)t1时刻后,NO2浓度降低,N2O4浓度增大,未到达平衡状态,反应向正反应进行.
解:(1)可逆反应2NO2N2O4的平衡常数表达式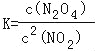 ,故答案为:
,故答案为: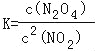 ;
;
(2)由图可知,从t1至t2时N2O4的物质的量变化量为4mol﹣3mol=1mol,故v(N2O4)=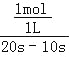 =0.1mol/(Ls),
=0.1mol/(Ls),
故答案为:0.1;
(3)到达平衡时,反应混合物各组分的物质的量不发生变化,由图象可知,t3时刻处于平衡状态,故答案为:t3;
(4)t1时刻后,NO2浓度降低,N2O4浓度增大,未到达平衡状态,反应向正反应进行,故正反应速率大于逆反应速率,
故答案为:>.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 聚氯乙烯塑料不可用来包装食品
B. 缺碘易患大脖子病
C. 由于淀粉在人体中会转化为氨基酸,因此每天都要摄入一定量的淀粉
D. 皮肤被烫伤或受浓硝酸腐蚀时,细胞结构将受到破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课题式研究性学习是培养学生创造思维的良好方法.某研究性学习小组将下列装置如图连接,D、F、X、Y 都是铂电极、C、E是铁电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
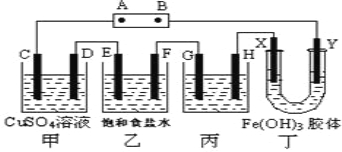
(1)电源B 极的名称是___________。
(2)甲装置中电解反应的总化学方程式是:_________________。
(3)设电解质溶液过量,则同一时间内C、D电极上参加反应的单质或生成的单质的物质的量之比是__________。
(4)欲用丙装置将粗铜(含少量铁、锌等杂质)精炼,G极材料应该是__________(填“粗铜”或“精铜”),电解液中原电解质的物质的量浓度将__________(填“变大”、“变小”或“不变”)。
(5)设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)反应aA(g)+bB(g)![]() cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
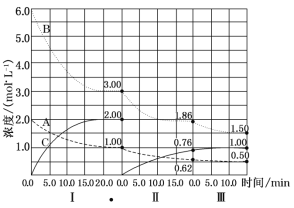
(1)反应的化学方程式中,a:b:c为_______;
(2)由第一次平衡到第二次平衡,改变的条件是__________;
(3) 由第二次平衡到第三次平衡,改变的条件是_________;
(4)第II阶段B的平衡转化率aII(B)=_______________;
(5)三次平衡时平衡常数KI、KII、KIII的大小顺序为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于镁的性质叙述正确的是( )
A.能在空气中燃烧,但不能在二氧化碳中燃烧
B.不能与氮气发生反应
C.不与冷水反应,但与热水反应
D.可用电解氯化镁溶液的方法来制取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍在电池、合金、催化剂等方面应用广泛.
(1)下列关于金属及金属键的说法正确的是 .
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是 .
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= .CO与N2结构相似,CO分子内σ键与π键个数之比为 .
(4)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为 ,甲醇分子内的O﹣C﹣H键角 (填“大于”“等于”或“小于”)甲醛分子内的O﹣C﹣H键角.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.因为Na2CO3+SiO2![]() Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
B.碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似
C.二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物
D.二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不和水反应生成硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述不正确的是
A.常温常压下,17g甲基(—14CH3)所含的中子数为8NA
B.0.1molFe与0.1molCl2充分反应,转移的电子数为0.2NA
C.标准状况下,44.8LNO与22.4LO2混合后气体的分子总数为2NA
D.1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com