(2012?石家庄一模)【化学一选修2:化学与技术】
现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高.其主要流程如下:
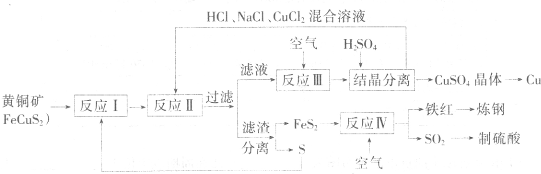
注:反应Ⅱ的离子方程式为Cu
2++CuS+4Cl
-=2[CuCl
2]
-+S
请回答:
(1)从黄铜矿冶炼粗铜的传统丁艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜、这种方法的缺点是
反应有SO2生成,易造成环境污染,同时消耗大量热能.
反应有SO2生成,易造成环境污染,同时消耗大量热能.
(2)反应Ⅰ的产物为(填化学式)
CuS、FeS2
CuS、FeS2
(3)反应Ⅲ的离子方程式为
4[CuCl2]-+O2+4H+=4Cu2++8Cl-+2H2O
4[CuCl2]-+O2+4H+=4Cu2++8Cl-+2H2O
(4)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
该温度下,硫酸铜的溶解度小于氯化铜
该温度下,硫酸铜的溶解度小于氯化铜
(5)黄铜矿中Fe的化合价为+2,关于反应.8CuFeS
2+21O
28Cu+4FeO+2Fe
2O
4+16SO
2下列说法正确的是
BCD
BCD
(填选项字母)
A.反应中被还原的元素只有氧
B.反应生成的SO
2直接排放会污染环境
C.SO
2既是氧化产物又是还原产物
D.当有8mol铜生成时,转移电子数目为100N
A(6)某硫酸厂为测定反应IV所得气体中SO
2的体积分数,取280mL(已折箅成标准状况)气体样品与足量Fe
2(SO
4)
3溶液完全反应后,用浓度为0.02000mol/L 的 K
2Cr
2O
2标准溶液滴定至终点,消耗K
2Cr
2O
3溶液25.00ml.
已知:Cr
2O
32-+Fe
2++H
+→Cr
3++Fe
3++H
2O(未配平)
①SO
2通入Fe
2(SO
4)
3溶液,发生反应的离子方程式为
SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
,
②反应Ⅳ所得气体中SO
2的体积分数为
12.00%
12.00%
.