
科目:高中化学 来源: 题型:
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
| 4 |
| 7 |
查看答案和解析>>
科目:高中化学 来源:江苏省淮阴中学2007届高三第一次阶段检测、化学 题型:022
| |||||||||||||||
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
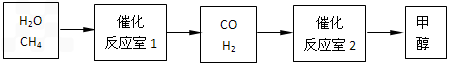
 CH3OH (g),CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH (g),CO的平衡转化率与温度、压强的关系如图所示,则: 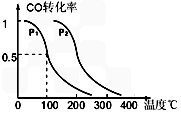
 CO(g) + 2H2(g)反应的平衡常数为________(用含a、V的代数式表示)
CO(g) + 2H2(g)反应的平衡常数为________(用含a、V的代数式表示)  SO3(g)+NO(g)上述反应,正反应速率随时间变化的趋势如图所示。由图可知下列说法正确的是__________(填字母)。
SO3(g)+NO(g)上述反应,正反应速率随时间变化的趋势如图所示。由图可知下列说法正确的是__________(填字母)。 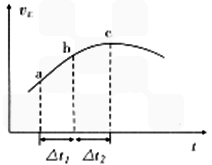
查看答案和解析>>
科目:高中化学 来源:陕西省模拟题 题型:填空题
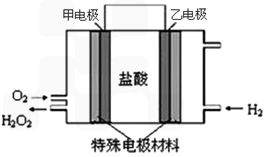
 2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。
2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。 
 CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题:
CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题: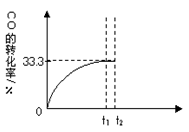
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)A、B、C、D、E、F六种元素,原子序数依次递增,其中A、B、C、D、E均为短周期元素。A元素原子核内无中子;B元素原子最外层电子数是次外层电子数的2倍;D是地壳中含量最高的元素;E和D同主族;F位于周期表的第四周期ⅠA族。根据以上信息用相关的元素符号回答下列问题:
⑴B与D形成化合物BD2的电子式为 。
⑵B、D、F三元素形成的化合物F2BD3的水溶液显碱性,溶液中各种离子物质的量浓度的大小顺序为(按从大到小的顺序排列) 。
⑶常温常压时,2.8g BD气体在3.2g D2气体中完全燃烧,生成BD2气体时放出28.3kJ的热量,则该热化学方程是 。
⑷A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式 。
⑸实验室中装有E最高价氧化物水化物浓溶液的试剂瓶应贴有的图标是
![]()

![]() a b c d
a b c d
⑹有人设想寻求合适的催化剂和电极材料,以C2、A2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。请写出该电池的正极反应式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com