
二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2 ,此方法制备得到的是纳米二氧化钛。
(1)① TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________;
② 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
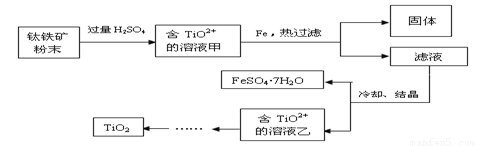
(2)Fe2O3与H2SO4反应的离子方程式是 。
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有 。
(4)加Fe的作用是 。
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
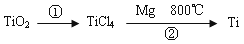
反应②的方程式是 ,该反应需要在Ar气氛中进行,请解释原因:_____________。
(1)①TiCl4+(x+2)H2O==TiO2•xH2O↓+4HCl②取最后一次洗涤液少量置于试管中,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净
(2)Fe2O3+6H+=2Fe3++3H2O
(3)Fe3+、Fe2+;
(4)将Fe3+转化为Fe2+
(5)TiCl4+2Mg=2MgCl2+Ti; 防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用.
【解析】
试题分析:(1)①设TiCl4的系数为1,根据元素守恒,TiO2•xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),方程式为TiCl4+(x+2)H2O⇌TiO2•xH2O↓+4HCl,②沉淀吸附溶液中的Cl-,根据发生反应:Cl-+Ag+═AgCl↓,取少量洗涤液,检验溶液中溶解的离子是否还存在;
(2)氧化铁和硫酸反应生成硫酸铁和水,离子方程式为:Fe2O3+6H+=2Fe3++3H2O,
(3)Fe2O3+6H+=2Fe3++3H2O,FeTiO3+4H+=Fe2++TiO2++2H2O,所以还存在的阳离子是Fe3+、Fe2+
(4)该溶液中含有铁离子,铁具有还原性,能将铁离子氧化生成亚铁离子且不引进新的杂质,所以铁的作用是:将Fe3+转化为Fe2+
(5)在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,反应方程式为:TiCl4+2Mg==2MgCl2+Ti ;Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气,防止Mg和空气中物质反应
考点:考查学生对工艺流程理解、阅读题目获取信息能力、氧化还原反应及方程式的书写等,难度中等,理解工艺流程是关键,需要学生具有阅读题目获取信息能力和灵活运用基础知识分析问题、解决问题能力.


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:

| ① |
| ② |
| Mg800℃ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年四川省高三上学期“一诊”模拟理综化学试卷(解析版) 题型:填空题
二氧化钛(TiO2)广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到胶体TiO2 ,此方法制备得到的是纳米二氧化钛。
(1)① TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________ ;
②检验TiO2·x H2O中Cl-是否被除净的方法是______________________________
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
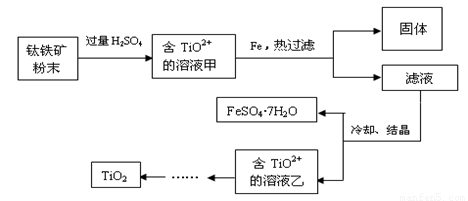
(2)钛铁矿粉末中加硫酸反应得TiO2+的离子方程式为
(3)溶液甲中加入Fe的作用是
(4)若要加热FeSO4.7H2O晶体得无水硫酸亚铁,除酒精灯、玻璃棒外,还要用到的两种硅酸盐质仪器是
Ⅱ二氧化钛可用于制取钛单质,涉及到的步骤如下图:
反应②的方程式是 ,该反应需要在Ar气氛中进行,请解释原因: _
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市昌平区高三上学期期末考试理综化学试卷(解析版) 题型:填空题
二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:

(1)Fe2O3与H2SO4反应的离子方程式是_________________________________。
(2)甲溶液中除含TiO2+之外还含有的金属阳离子有__________________。
(3)加Fe的作用是_________________________________。
方法2:TiCl4水解生成TiO2·x H2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2 ,此方法制备得到的是纳米二氧化钛。
(4)① TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________;
② 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
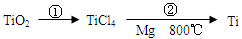
反应②的方程式是 ,该反应需要在Ar气氛中进行,请解释原因:_____________。
查看答案和解析>>
科目:高中化学 来源:2010年浙江省高二第二学期期中考试(1-3班)化学试题 题型:填空题
(19分)高锰酸钾是锰的重要化合物和常用的氧化剂。以下是实验室中模拟工业上用软锰矿制备高锰酸钾的流程图。
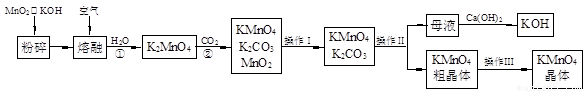
(1)操作Ⅰ的名称为 ;操作Ⅲ的名称为 。
(2)反应②的化学方程式为 。工业上用上述原理生产KMnO4方法产率较低,较好的制备方法是电解法。用Pt作阳极,Fe作阴极,K2MnO4为电解液,阳极的电极反应式为 。
(3)KMnO4是一种较稳定的化合物,但日光对KMnO4溶液的分解有催化作用,生成MnO2、KOH和O2。而 MnO2也是该分解反应的一种催化剂,请你设计一个实验方案,验证MnO2对该分解反应具有催化性: 。
(4)KMnO4在酸性介质中的强氧化性广泛应用于分析化学中。
例如:2KMnO4+3H2SO4+5Na2SO35Na2SO4+K2SO4+2MnSO4+3H2O。某同学用KMnO4测定实验室长期存放的Na2SO3固体的纯度。现欲准确称取6.3 g Na2SO3固体样品,配成500 mL溶液。取25.00 mL上述溶液放入锥形瓶中,用0.01000 mol/L 的酸性KMnO4溶液进行滴定。滴定结果如下表所示:
|
滴定次数[来源:][来源:Z&xx&k.Com] |
待测溶液的体积/mL[来源:学#科#网Z#X#X#K] |
标准溶液的体积[来源:] |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
1 |
25.00 mL |
0.02 |
24.01 |
|
2 |
25.00 mL |
0.70 |
24.71 |
|
3 |
25.00 mL |
0.20 |
24.20 |
①配制500 mLNa2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、胶头滴管、药匙和 、 。
②判断滴定终点的依据是 。
③下列操作会导致测定结果偏高的是
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.滴定前锥形瓶未干燥
C.滴定前滴定管尖嘴部分有气泡
D.观察读数时,滴定前仰视,滴定后俯视
④用上述实验数据,计算Na2SO3的纯度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com