
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
①上述反应符合“原子经济”原则的是________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
温度 | 250 ℃ | 300 ℃ | 350 ℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断,ΔH1______0(填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为________(从上表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:__________。
(1)①Ⅰ ②< ③80% 250 ℃
(2)CH3OH(l)+O2(g)===CO(g)+2H2O(l)
ΔH=-442.8 kJ·mol-1
【解析】 (1)①反应Ⅰ的产物只有甲醇,而反应Ⅱ的产物有两种,故反应Ⅰ符合“原子经济”原则;②观察图表数据可得,升温时,K值变小,说明该反应的正反应为放热反应,即ΔH1<0;③CO的转化率为(2 mol-0.2 mol·L-1×2 L)/2 mol×100%=80%;此时的化学平衡常数为K=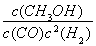 =
=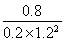 ≈2.041,故此时的温度为250 ℃。(2)将三个热化学方程式进行变形:[①+(-②)+4×③]×
≈2.041,故此时的温度为250 ℃。(2)将三个热化学方程式进行变形:[①+(-②)+4×③]×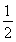 ,可得甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式,即CH3OH(l)+O2(g)===CO(g)+2H2O(l) ΔH=[ΔH1+(-ΔH2)+4ΔH3]×
,可得甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式,即CH3OH(l)+O2(g)===CO(g)+2H2O(l) ΔH=[ΔH1+(-ΔH2)+4ΔH3]×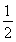 =-442.8 kJ·mol-1。
=-442.8 kJ·mol-1。


 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题8电化学原理练习卷(解析版) 题型:选择题
将KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是 ( )。

A.整个过程中两电极反应2Cl--2e-===Cl2↑、2H++2e-===H2↑不可能同时发生
B.电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度
C.ab段表示电解过程中H+被还原,pH上升
D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题6化学反应速率和化学平衡练习卷(解析版) 题型:填空题
25 ℃时,在体积为2 L的密闭容器中,气态A、B、C的物质的量n随时间t的变化如图1所示,已知达到平衡后,降低温度,A的转化率将增大。

t2~t3 | t4~t5 | t5~t6 | t7~t8 |
K1 | K2 | K3 | K4 |
(1)根据图1数据,写出该反应的化学方程式:__________________。此反应的平衡常数表达式K=___,从反应开始到第一次平衡时的平均速率v(A)为___。
(2)在5~7 min内,若K值不变,则此处曲线变化的原因是__________。
(3)如图2表示此反应的反应速率v和时间t的关系图,各阶段的平衡常数如表所示。K1、K2、K3、K4之间的关系为________(用“>”、“<”或“=”连接)。A的转化率最大的一段时间是________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题6化学反应速率和化学平衡练习卷(解析版) 题型:选择题
在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3— (aq)。测得不同温度下该反应的平衡常数K如表所示:
I3— (aq)。测得不同温度下该反应的平衡常数K如表所示:
t/℃ | 5 | 15 | 25 | 35 | 50 |
K | 1 100 | 841 | 689 | 533 | 409 |
下列说法正确的是 ( )。
A.反应I2(aq)+I-(aq) I3— (aq)的ΔH>0
I3— (aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I3—)减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题5化学反应与能量变化练习卷(解析版) 题型:选择题
(2013·广东中山一模,11)下列依据热化学方程式得出的结论正确的是(双选)( )。
A.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1
B.已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量
C.已知2C(s)+2O2(g)===2CO2(g) ΔH=a;2C(s)+O2(g)===2CO(g) ΔH=b,则a>b
D.已知C(石墨,s)===C(金刚石,s) ΔH>0,则石墨比金刚石稳定
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题4物质结构与元素周期律练习卷(解析版) 题型:填空题
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________;M在元素周期表中的位置为________;五种元素的原子半径从大到小的顺序是________(用元素符号表示)。
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,A的电子式为________,B的结构式为________。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为________,该族二~五周期元素单质分别与H2反应生成1 mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是________(填字母代号)。
a.+99.7 kJ·mol-1 b.+29.7 kJ·mol-1c.-20.6 kJ·mol-1 d.-241.8 kJ·mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出阳极生成R的电极反应式:____________________________________;由R生成Q的化学方程式为________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题3中学化学常见的两种重要反应类型练习卷(解析版) 题型:选择题
下列离子方程式正确的是(双选)( )。
A.氯化铁溶液中加入铜粉:2Fe3++Cu===2Fe2++Cu2+
B.向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+===Fe2++2H2O
C.硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42—===BaSO4↓
D.向硫酸氢钠溶液中滴加Ba(OH)2溶液至中性:2H++SO42—+Ba2++2OH-===BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题1物质的组成分类性质及化学用语练习卷(解析版) 题型:选择题
下列叙述正确的是( )。
A.盐酸和食醋既是化合物又是酸
B.纯碱、CuSO4·5H2O和生石灰分别属于盐、混合物和氧化物
C.胶体处于介稳定状态,所以放置一会便会有沉淀生成
D.胶体区别于其他分散系的本质特征是分散质粒子直径的大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com