
已知25℃时:
① NH4+ (aq) 十OH—(aq)=NH3·H2O(aq) ΔH=a kJ·mol-1
② NH4+
(aq) 十H2O(1)  NH3·H2O(aq)十H+(aq) ΔH=bkJ·mol-1
NH3·H2O(aq)十H+(aq) ΔH=bkJ·mol-1
向20 mL0.1mol/L氨水中逐滴加入0.1mol/L盐酸,下列有关说法正确的是( )
A.随着盐酸的逐滴加入,水电离的c(OH—)总是逐渐减小
B.当滴入10mL盐酸时,溶液中:c(NH4+)十c(NH3·H2O)=2c(Cl—)
C.当滴入20mL盐酸时,溶液中:c(Cl—)十c(H+)=c(NH4+)十c(OH—)
D.水电离过程的热化学方程式可表示为:H2O(1)
 H+(aq)+OH—(aq) ΔH=( b-a) kJ·mol-1
H+(aq)+OH—(aq) ΔH=( b-a) kJ·mol-1
BD
【解析】
试题分析:氨水溶液显碱性,对水的电离起到抑制作用,随着盐酸的加入,OH-的浓度逐渐减小,则水的电离程度逐渐增大,故A错误;由于氨水的浓度等于盐酸的浓度,所以当滴入10mL盐酸时,根据物料守恒c(NH4+)十c(NH3·H2O)=2c(Cl—),B正确;当滴入20mL盐酸时,恰好完全反应,氯化铵水解呈酸性c(Cl—)>
c(NH4+)、 c(H+)>c(OH—),所以c(Cl—)十c(H+)>c(NH4+)十c(OH—),C错误;根据盖斯定律,由已知的两个方程式②-①得水电离得热化学方程式H2O(1)
 H+(aq)+OH—(aq) ΔH=( b-a) kJ·mol-1,所以D正确;故选BD。
H+(aq)+OH—(aq) ΔH=( b-a) kJ·mol-1,所以D正确;故选BD。
考点:本题考查的是强酸弱碱的混合、盐类的水解、盖斯定律的应用等知识。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
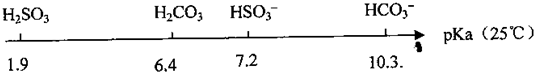
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数:则下列有关说法正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三种物质在常温下溶解度最小的是AgI | B、饱和AgCl溶液中,c(Ag+)≈1.34×10-5mol/L | C、将氯化银置于饱和KI溶液中,固体慢慢会由白色转化为黄色 | D、将浓度均为1×10-6mol/L的AgNO3溶液、KBr溶液等体积混合会生成沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com