
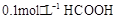 溶液加水不断稀释,下列各量始终保持增大的是( )
溶液加水不断稀释,下列各量始终保持增大的是( )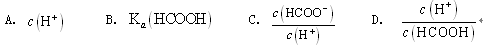
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.甲、乙两溶液的c(H+)之比为400︰1 |
| B.甲、乙两溶液均呈酸性 |
| C.甲中水的电离程度小于乙中水的电离程度 |
| D.甲中水的电离程度与乙中水的电离程度无法比较 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(K +)+c(H+)= c(OH-)+ c(HS-)+2 c(S2-) | B.c(K+)> c(HS-)> c(OH-)> c(S2-)> c(H+) |
| C.c(HS-)+ c(S2-)+ c(H2S)=" 0.1" mol?L-1 | D.c(K+)> c(HS-)> c(OH-)> c(H2S)> c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.①② | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 L,pH= .
L,pH= . 体积的变化),测得混合溶液的pH=6,试回答以下问题:
体积的变化),测得混合溶液的pH=6,试回答以下问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。  时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题: 字):
字):查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ________25 ℃。
________25 ℃。 H =11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),所得混合液为中性,求a∶b等于多少?
H =11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),所得混合液为中性,求a∶b等于多少?查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com