
【题目】2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___,基态磷原子中,电子占据的最高能层符号为___;该能层能量最高的电子云在空间有___个伸展方向,原子轨道呈___形。
(2)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为__,该配离子中各元素的第一电离能由小到大的顺序为___(填元素符号),1mol该配离子中含σ键数目为___NA。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
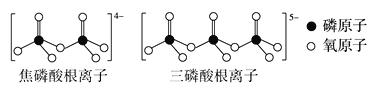
这类磷酸根离子的化学式可用通式表示为___(用n代表P原子数)。
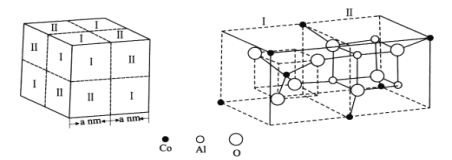
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___,晶体中Al3+占据O2-形成的___(填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数的值,钴蓝晶体的密度为___g·cm-3(列计算式)。
【答案】1s22s22p63s23p63d74s2或[Ar]3d74s2 M 3 哑铃 sp2 Co、O、N 16 (PnO3n+1)(n+2)- CoAl2O4 八面体空隙 ![]()
【解析】
(1)Co为27号元素,Co原子核外有27个电子,根据核外电子排布规律可得其基态Co原子核外电子排布式;基态磷原子核外有三层电子,故最高能层符号为M,电子云在空间有3个伸展方向,原子轨道为哑铃型,故答案为:1s22s22p63s23p63d74s2或[Ar]3d74s2;M;3;哑铃;
(2)NO3-中价层电子对数为![]() ,故为sp2杂化;一般情况下非金属性越强第一电离能越大,但由于N原子中最外层为半充满状态,比较稳定,故第一电离能大于O,所以第一电离能由小到大的顺序为Co、O、N;一个NO3-中有3个σ键,配位键也为σ键,故σ键数目为3×4+4=16,则1mol该配离子中含σ键数目为16NA,故答案为:sp2;Co、O、N;16;
,故为sp2杂化;一般情况下非金属性越强第一电离能越大,但由于N原子中最外层为半充满状态,比较稳定,故第一电离能大于O,所以第一电离能由小到大的顺序为Co、O、N;一个NO3-中有3个σ键,配位键也为σ键,故σ键数目为3×4+4=16,则1mol该配离子中含σ键数目为16NA,故答案为:sp2;Co、O、N;16;
(3)可以根据磷酸根、焦磷酸根、三磷酸根的化学式推导:PO43-、P2O74-、P3O105-磷原子的变化规律为:1,2,3,4,n氧原子的变化规律为:4,7,10,3n+1 酸根所带电荷数的变化规律为:3,4,5,n+2;故答案为:(PnO3n+1)(n+2)-
(4)根据钴蓝晶体晶胞结构分析,一个晶胞中含有的Co、Al、O个数分别为:![]() ,
,![]() ,
,![]() ,所以化学式为CoAl2O4;根据结构观察,晶体中Al3+占据O2-形成的八面体空隙;该晶胞的体积为
,所以化学式为CoAl2O4;根据结构观察,晶体中Al3+占据O2-形成的八面体空隙;该晶胞的体积为![]() ,该晶胞的质量为
,该晶胞的质量为![]() ,所以密度为
,所以密度为 ![]() ,故答案为:CoAl2O4;八面体空隙;
,故答案为:CoAl2O4;八面体空隙;![]() 。
。


科目:高中化学 来源: 题型:
【题目】现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片。请回答下列问题:
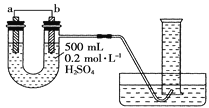
(1)b电极反应式为___。
(2)当量筒中收集到672mL(标准状况下)气体时,通过导线的电子的物质的量为__,此时a电极质量减少____g。
(3)如果将a、b两电极的电极材料对调,U形管中将出现的现象是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型化学实验能有效减少污染,节约药品。下图中,某学生在衬有一张白纸的玻璃片上放置表面皿,在表面皿上的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,在表面皿中心处放置2小粒KMnO4晶体,并滴加一滴浓盐酸,立即将表面皿盖好。可见KMnO4晶体很快溶解,并产生气体。

(1) 完成本实验中制取Cl2的化学方程式:
__KMnO4+____HCl(浓)—___KCl +_____ MnCl2 + ____ Cl2↑+__ ______ .
如该反应中消耗还原剂的物质的量为8mol,则电子转移数目为________ .
⑵b处的实验现象为___________;c处的实验现象为____________
⑶d处反应的离子方程式为_______、_______
⑷通过该实验能比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱,其氧化性由强到弱的顺序是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物同分异构体说法中错误的是
A. 三联苯(![]() )的一氯代物有4种
)的一氯代物有4种
B. 立方烷(![]() )经硝化可得到六硝基立方烷,其可能的结构有3种
)经硝化可得到六硝基立方烷,其可能的结构有3种
C. β-月桂烯(![]() )与溴发生1:1加成反应,产物(只考虑位置异构)有3种
)与溴发生1:1加成反应,产物(只考虑位置异构)有3种
D. 酯类化合物C4H8O2在酸性条件下水解得到的醇可能有4种不同结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
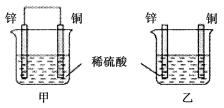
①两烧杯中铜片表面均无气泡产生
②甲中铜片是正极,乙中铜片是负极
③两烧杯中溶液的c(H+)均减小
④产生气泡的速率甲比乙慢
⑤甲中SO42-向Zn片移动,H+向Cu片移动
⑥乙中电流从Cu片流向Zn片
⑦甲乙两烧杯中Cu片的质量均不变
A. ①②③B. ③⑤⑦
C. ④⑤⑥D. ②③④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释到100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为______mol·L-1。
84消毒液
有效成分:NaClO
规格:1000 mL
质量分数:25%
密度:1.19 g·cm-3
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL该物质的量浓度的消毒液。下列说法正确的是_____(填字母)。

A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于配制溶液
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g
(3)“84消毒液”与稀盐酸混合会产生一种黄绿色的气体,写出反应的离子方程式:_____
(4)钛铁矿(主要成分为FeTiO3,Ti为+4价)加盐酸“酸浸”后,钛主要以TiOCl42-形式存在,写出反应的离子方程式:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家从化肥厂生产的(NH4)2SO4中检出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42- 和N4H44+ 两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子,N4分子不能被植物吸收。请回答下列问题:

(1)下列相关说法中,正确的是________(填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 molπ键
c.白磷的沸点比N4高,是因为P-P键键能比N-N键能大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
(2)叠氮化物是研究较早的含全氮阴离子的化合物,如:氢叠氮酸(HN3)、叠氮化钠(NaN3)等。根据等电子体理论写出N3- 的电子式_______;叠氮化物能形成多种配合物,在[Co(N3)(NH3)5]SO4,其中钴显 ____ 价,它的配体是 __________
(3)六方相氮化硼晶体内B-N键数与硼原子数之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列各题:
(1)![]() 中非含氧官能团的名称是_______;含氧官能团的电子式为_______。
中非含氧官能团的名称是_______;含氧官能团的电子式为_______。
(2)![]() 的系统命名为_______。
的系统命名为_______。
(3)写出CH3CH2CHO的银镜反应方程式:_______。
(4)2,6-二甲基-4-乙基辛烷的结构简式为_______,1 mol该烃完全燃烧需消耗氧气_______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com