
【题目】下列物质间不能发生离子反应的是
A. Na2SO4溶液与BaCl2溶液 B. NaOH溶液和稀H2SO4溶液
C. NaCl溶液与KNO3溶液 D. Na2CO3溶液与稀盐酸溶液
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 二氧化锰和浓盐酸反应:MnO2+4H++4Cl- ![]() Mn2++2Cl2+2H2O
Mn2++2Cl2+2H2O
B. 往NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
C. 往酸性碘化钾溶液中滴加适量的双氧水:2H++2I-+H2O2=I2↑+2H2O
D. 向NaHSO4溶液中滴加Ba(OH)2溶液反应至中性:H++SO42+ Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的装置进行实验。通入SO2气体,将带火星的木条插入试管C中的溶液上方,木条复燃。
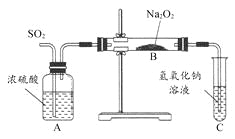
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是 。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3: 。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理? 。请简要说明两点理由:① ;② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸锂(Li2TiO3)白色粉末、熔点1520~1564℃、不溶于水,具有极强的助溶性质。利用锂辉石(主要成份Li2O·Al2O3·4SiO2,含有少量杂质MgO、Fe2O3等)制备钛酸锂的流程如下:

(1)钛酸锂(Li2TiO3)中钛元素化合价为________。
(2)对锂辉石进行焙烧主要目的之一是使Al2O3变性而不与酸反应,为了焙烧充分可以采取的措施是_____________。(写一条即可)
(3)写出酸浸时Fe2O3与H2SO4反应的离子方程式__________。
(4)水浸时加入碳酸钙是调整pH,主要使____________(填离子符号)沉淀。滤渣B为MgCO3、______、________(填化学式)。
( Ksp[Mg(OH)2]=1.8×10-11、Ksp[MgCO3]=6.8×10-6、Ksp[Fe(OH)3]=4.0×10-38)
(5)步骤①中控制H2TiO3与LiOH·H2O物质的量之比为____投料即可。
(6)新型钛酸锂Li4Ti5O12是“寿命最长”的电池负极材料,当Li+迁入时,该电极则_____(填“得到电子”或“失去电子”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
A.分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B.分子中的所有原子均达到8电子稳定结构
C.NCl3分子是非极性分子
D.NBr3比NCl3易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知次氯酸分子的结构式为H—O—Cl,下列有关说法正确的是( )
A. O原子发生sp杂化 B. 该分子的电子式是H︰O︰Cl
C. 该分子为直线型分子 D. O原子与H、Cl都形成σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一,
可采用苯乙腈为原料在实验室进行合成。请回答:
(1)制备苯乙酸的装置如图(加热和夹持装置等略)。已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。

在250mL三口瓶a中加入70mL质量分数为70%的硫酸,加热至100℃,再缓缓滴入40g苯乙腈,然后升温至130℃,发生反应:

仪器b的名称是______________,其作用是______________。反应结束后加适量冷水再分离出苯乙酸粗品,加入冷水的目的是___________________________________。
(2)分离出粗苯乙酸的操作名称是______,所用到的仪器是(填字母)______。
a.漏斗 b.分液漏斗 c.烧杯 d.玻璃棒 e.直形冷凝管
(3)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后加入Cu(OH)2,搅拌30min,过滤,滤液静置一段时间可以析出苯乙酸铜晶体,写出发生反应的化学方程式__________________,混合溶剂中乙醇的作用是________________________________________________________。
(4)提纯粗苯乙酸最终得到44g纯品,则苯乙酸的产率是_________。
(相对分子质量:苯乙腈 117,苯乙酸 136)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)![]() MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是( )
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是( )
A. 若降温,该反应的平衡常数增小
B. 吸收y mol H2只需1 mol MHx
C. 容器内气体密度保持不变
D. 若向容器内通入少量氢气,则v(放氢)>v(吸氢)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com