
| A����ع���ʱ���������� |
| B����ظ����ĵ缫��ӦʽΪ��3O2��6H2O��12e����12OH�� |
C����ع���ʱ������������ͨ�����·���� |
| D�����·��ÿͨ��1mol e�����������������ϼ�С9g |
 ��������������������ϵ�д�
��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��p�ܼ���ԭ�ӹ���������Σ������ܲ�����ӣ�p�ܼ�ԭ�ӹ��Ҳ������ |
| B���õ�ⷨ������ͭʱ����ͭ������ |
| C��ǿ�������Һ�ĵ�������һ�������������Һǿ |
| D��Ǧ�����ڷŵ�����У������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

| ������ | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | �ݨC0.42 | ��2.5 | ��7 | ��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������п�̵���Ƕ��ε�� |
| B��������ӦΪ��2 MnO2��2H2O��2e����2MnOOH��2OH�� |
| C������������ļ���п�̵���е��Һ��pH����С |
| D�������У�ÿת��0.2mole��ʱ��������������6.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ӧʽ��O2+2H2O+4e����4OH�� |
| B��������Ӧʽ��CH4+8OH����8e����CO2��+6H2O |
| C�����ŷŵ�Ľ��У���Һ��pHֵ���� |
| D���ŵ�ʱ��Һ�е����������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


| ���� | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 |
| ��ʼ����pH | 2.7 | 7.6 | 5.7 | 8.3 |
| ��ȫ����pH | 3.7 | 9.6 | 8.0 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ȼ�ϵ����ͨ��ȼ�շ�ʽ����ѧ��ת��Ϊ���� |
| B������ȼ�ϵ���У�ͨ��������һ��Ϊ���� |
| C��������ȼ��ʱ������Ϊ������̼��ˮ |
| D��ȼ�ϵ�ص�����ת���ʿɴ�100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��пͲ������������������Ӧ |
| B�����Ӵ�п����̼����̼���õ��ӱ���ԭ |
| C������ڲ���NH4+ ��̼���ƶ� |
| D����NH4Cl����ΪKOH����ߵ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH| A���ŵ�ʱÿת��6mol���ӣ�������2mol K2FeO4����ԭ |
| B�����ʱ������ӦΪ��Zn(OH)2 + 2e�� = Zn+ 2OH�� |
C���ŵ�ʱ������ӦΪ��FeO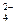 + 3e�� + 4H2O = Fe(OH)3 + 5OH�� + 3e�� + 4H2O = Fe(OH)3 + 5OH�� |
| D�����ʱZn�缫�����Դ�ĸ������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com