
 2NO2
2NO2 
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:多选题
| A.3mol和70% | B.2mol和80% | C.2mol和70% | D.4mol和70% |
查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题
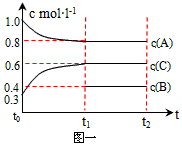
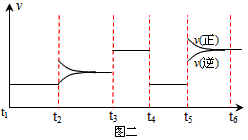
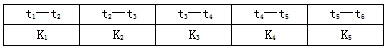
查看答案和解析>>
科目:高中化学 来源:杭州二模 题型:填空题
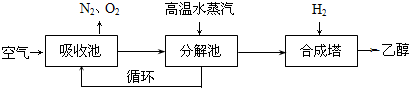
| 温度(K) CO2转化率(%) n(H2)/n(CO2) |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
| n(H2) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源:同步题 题型:不定项选择题
 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%.其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%.其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 查看答案和解析>>
科目:高中化学 来源:同步题 题型:不定项选择题
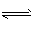 C(g)+3D(g),现从两条途径分别建立平衡。
C(g)+3D(g),现从两条途径分别建立平衡。[ ]
查看答案和解析>>
科目:高中化学 来源:专项题 题型:单选题
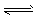 2SO3 (g) ; △H = - 196.6 kJ/mol时,下列六种说法中正确的有
2SO3 (g) ; △H = - 196.6 kJ/mol时,下列六种说法中正确的有查看答案和解析>>
科目:高中化学 来源:0101 期中题 题型:单选题
 N2+3H2,达平衡时,N2的物质的量分数为a %,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a %的是
N2+3H2,达平衡时,N2的物质的量分数为a %,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a %的是 查看答案和解析>>
科目:高中化学 来源:专项题 题型:单选题
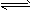 2HI(g) △H<0。有相同容积的定容密封容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
2HI(g) △H<0。有相同容积的定容密封容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com