
反应H2(g)+CO2(g)![]() H2O(g)+CO(g),在773 K时,平衡常数K=9.如反应开始时,CO和H2O的浓度都是0.020 mol·L-1,计算在此条件下CO的转化率.
H2O(g)+CO(g),在773 K时,平衡常数K=9.如反应开始时,CO和H2O的浓度都是0.020 mol·L-1,计算在此条件下CO的转化率.
 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________________________;
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇(CO2+3H2CH3OH + H2O)
在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);下列说法正确的是______(填序号)
①温度为T1时,从反应开始到平衡,
生成甲醇的平均速率为v(CH3OH)=nA/tA mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)/n(CH3OH)增大
(4)在T1温度时,将1mol CO2和3mol H2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为_________________________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省武汉市三角路中学高二上学期期末考试化学试卷 题型:填空题
能源是人类生存和发展的重要支柱。研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义。
(1)已知下列热化学方程式:
① H2(g)+1/2O2(g) =H2O(g) ΔH=-241.8 kJ/mol
② C(s)+1/2O2(g) =CO(g) ΔH=-110.5 kJ/moL
则水煤气能源的制取原理:C(s)+H2O(g)=H2(g)+CO (g) ΔH= kJ/moL
(2)研究活化能对于能源技术的革新有非常重大的实际意义。请认真观察下图,回答问题:
① 图中反应的ΔH= kJ/mol(用含有E1、E2代数式表示)。
② 已知热化学 方程式:H2(g)+1/2O2(g) = H2O(g) ΔH=-
方程式:H2(g)+1/2O2(g) = H2O(g) ΔH=- 241.8 kJ/mol,该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为 kJ/mol。
241.8 kJ/mol,该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为 kJ/mol。
③ 图中虚线(II)与实线(I) 对于同一反应具有的意义:
。
查看答案和解析>>
科目:高中化学 来源:2013届江西省高二下学期教学竞赛化学试卷(解析版) 题型:选择题
某温度下,C和H2O(g)在密闭容器里发生下列反应:
C(s)+H2O(g) CO(g)+H2(g), CO(g)+H2O(g)
CO(g)+H2(g), CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,c(H2)=1. 9 mol·L-1,c(CO)=0. 1 mol·L-1。则下列叙述正确的有
A. CO在平衡时转化率为10%
B. 平衡浓度c(CO2)=c(H2)
C. 平衡时气体平均相对分子质量约为23.3
D. 其他条件不变时,缩小体积,H2O(g)的转化率随之降低
查看答案和解析>>
科目:高中化学 来源:2012届浙江省台州市高二下学期期末测试化学 题型:选择题
在恒容密闭容器中存在下列平衡:C(s)+H2O(g) CO(g)+H2(g)。CO(g)的平衡物质的量浓度c(CO)与温度T的关系如右图所示。下列说法错误的是
CO(g)+H2(g)。CO(g)的平衡物质的量浓度c(CO)与温度T的关系如右图所示。下列说法错误的是

A.该反应的ΔH>0
B.若T1、T2时的平衡常数分别为K1、K2,则K1=K2
C.通过加热可以使B点变到C点
D.在T2时若反应进行到状态D,则一定有υ(正) <υ(逆)
查看答案和解析>>
科目:高中化学 来源:2012届浙江省高二下学期期末考试化学试卷 题型:选择题
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol液态水消耗的能量是__________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________________________________;
(3)在容积为2L的密闭容器中,由一定量的CO2和H2合成甲醇,在其他条件不变的情况下,温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);下列说法正确的是___________(填序号)
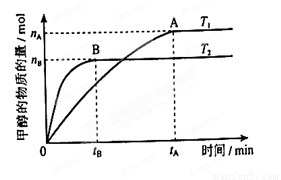
① 温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)= 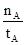 mol·L-1·min-1
mol·L-1·min-1
② 该反应在T1时的平衡常数比T2时的大
③ 该反应的 △H < 0
④ 处于A点的反应体系从T1变到T2,达到平衡时容器中气体密度减小
⑤ 处于A点时容器中的压强比处于B点时容器中的压强大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a, 则容器内的压强与起始压强之比为___________;
(5)在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com