
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:
Ⅰ.R1COOR2+ R318OH![]() R1CO18OR3+R2OH(R1、R2、R3代表烃基)
R1CO18OR3+R2OH(R1、R2、R3代表烃基)
![]() Ⅱ.
Ⅱ. (R4、R5代表烃基)
(R4、R5代表烃基)
(1)①的反应类型是 。
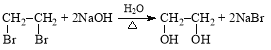
(2)②的化学方程式为 。
(3)PMMA单体的官能团名称是 、 。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为 。
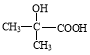
(5)G的结构简式为 。
(6)下列说法正确的是 (填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.1 mol  与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是 。
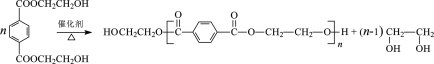
(8)写出由PET单体制备PET聚酯并生成B的化学方程式 。
【答案】(1)加成反应
(2)
(3)碳碳双键 酯基
(4)![]()
(5)
(6)a
(7)
(8)
【解析】
试题解析:根据题中各物质转化关系,由PMMA的结构可知,PMMA单体为CH2=C(CH3)COOCH3,E氧化得F,F的核磁共振氢谱显示只有一组峰,F发生信息Ⅱ中的反应得G,G在浓硫酸作用下发生消去反应得J,结合PMMA单体的结构和E的分子式可知,E为CH3CH(OH)CH3,F为CH3COCH3,G为(CH3)2C(OH)COOH,J为CH2=C(CH3)COOH,所以D为CH3OH,乙烯与溴发生加成反应生成A为BrCH2CH2Br,A在碱性条件下水解得B为HOCH2CH2OH,B与对苯二甲酸甲酯发生信息Ⅰ的反应生成PET单体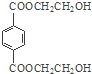 和D(CH3OH),PET单体发生缩聚反应得PET聚酯。
和D(CH3OH),PET单体发生缩聚反应得PET聚酯。
(1)根据上面的分析可知,反应①的反应类型是加成反应
(2)②的化学方程式为 ![]() 。
。
(3)PMMA单体为CH2=C(CH3)COOCH3,PMMA单体的官能团名称是碳碳双键和酯基。
(4)反应⑤是E[CH3CH(OH)CH3]生成F(CH3COCH3)的反应,该反应为氧化反应,化学方程式为:
![]() 。
。
(5)根据以上分析可知G的结构简式为 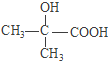 。
。
(6)a.⑦为CH2=C(CH3)COOH与HOCH3发生酯化反应,故a正确;b.D为CH3OH,B为HOCH2CH2OH,
它们的羟基的数目不同,所以B和D不是互为同系物,故b错误;c.1mol 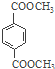 与足量NaOH溶
与足量NaOH溶
液反应时,最多消耗2mol NaOH,故c错误。
(7)J为CH2=C(CH3)COOH,碳碳双键在碳链一端时没有顺反异构,J的某种同分异构体与J具有相同官
能团,且为顺式结构,则碳碳双键应在碳链中间,其结构简式是![]() 。
。
(8)由PET单体制备PET聚酯是缩聚反应,根据题意要求,应该缩去小分子乙二醇,化学方程式为
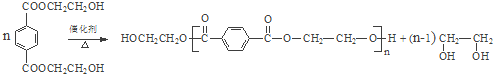 。
。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】研究表明,化学反应的能量变化与反应物和生成物的键能有关。键能可以简单的理解为断开1mol化学键时所需吸收的能量。下表是部分化学键的键能数据
化学键 | P—P | P—O | O=O | P=O |
键能 kJ·mol-1 | 197 | 360 | 499 | X |
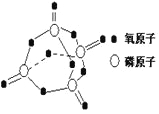
己知白磷的燃烧方程式为:P4(s)+5O2(g)=P4O10(s),该反应放出热量2378.0kJ ,且白磷分子结构为正四面体,4 个磷原子分别位于正四面体的四个顶点,白磷完全燃烧的产物结构如上图所示,则上表中X为
A.434 B.335 C.237 D.188
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
F、G都是常见的高分子材料,以下是由丙烯合成F、G的流程图。
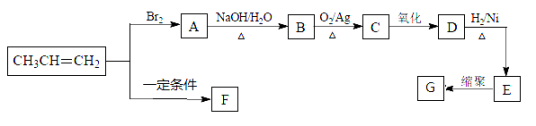
(1)E的化学名称是 ,所含官能团是 。
(2)G的结构简式是 。
(3)A→B的化学方程式是 ,该反应类型是 。
(4)由CH3CH=CH2生成F的化学方程式是 ,该反应类型是 。
(5)在一定条件下,两分子E脱去两分子水形成一种六元环状化合物,该化合物的结构简式是 。
(6)C的同分异构体有多种,请分别写出符合下列条件有机物的结构简式:
①能与NaHCO3溶液反应的是 ;
②能发生水解反应的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2Zn(OH)2ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2、Mn2+等离子)为原料制备2Zn(OH)2ZnCO3的工艺流程如下:
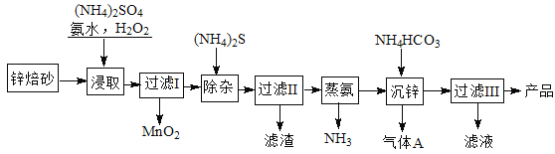
请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液呈中性时, c(NH4+) 2c(SO42-)(填“<”、“>”或“=”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是 (任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为 。
(4)适量S2能将Cu2+等离子转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: 。
[已知:Ksp(ZnS)=1.6×1024,Ksp(CuS)=1.3×1036+;K﹥105化学反应完全]
(5)“沉锌”的离子方程式为 。
(6)“过滤3”所得滤液可循环使用,其主要成分的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素的离子都和氩原子具有相同的电子层排布。X元素单质能在氢气中燃烧,产生苍白色火焰;Y元素氢化物的分子式是H2Y,其最高氧化物含有40%的Y;Z元素的离子具有紫色的焰色反应。
(1)根据以上条件,推断元素名称:X:_____,Y:_____,Z:________。
(2)X、Y、Z最高价氧化物对应的水化物的酸性由强到弱的顺序是________。
(3)用电子式表示Z2Y的形成过程:___________,其化合物中化学键的类型是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的说法正确的是( )。
A. 可用25mL碱式滴定管量取20.00mL KMnO4溶液
B. 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C. 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全
D. 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的![]() ,液体也不能蒸干
,液体也不能蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜元素能形成多种化合物。
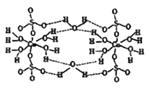
(1)写出基态Cu的M能层的电子排布式 ,Cu同周期的元素中,与铜原子最外层电子数相等的元素还有 (填元素符号)
(2)CuSO4·5H2O也可写成[Cu(H2O)4]SO4·H2O,其结构示意图如右图所示:该晶体中所含元素电负性由大到小顺序是 ,该晶体属于 晶体,该晶体中由水分子参与形成的作用力有 。
(3)Cu2+能与NH3、Cl-等形成配位数为4的配合物,已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 ,NH3的VSEPR 模型为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
(除特别注明外,其它一律用化学式表示)

(1)在这些元素中,化学性质最不活泼的是: (填具体元素符号,下同),其原子结构示意图为 。元素K名称为 在周期表中的位置 。
(2)最高价氧化物水化物中碱性最强的化合物的电子式是: 。]
(3)某元素二价阳离子的核外有10个电子,该元素是 (填元素名称)
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序
(5)F、H、J的最高价氧化物对应水化物的酸性由强到弱的顺序 。
(6)I、J、K三种元素形成的离子,离子半径由大到小的顺序是 。
(7)元素I的氢化物的结构式为 ;该氢化物常温下和元素K的单质反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:一定条件下,向一个密闭容器中加入0.30molX、0.10molY和一定量的Z三种气体,甲图表示发生反应后各物质浓度(c)随时间(t)的变化〔其中t0~t1阶段c(Z)未画出〕。乙图表示化学反应速率(v)随时间(t)的变化,四个阶段都只改变一种条件(催化剂、温度、浓度、压强,每次改变条件均不同),已知t3~t4阶段为使用催化剂。
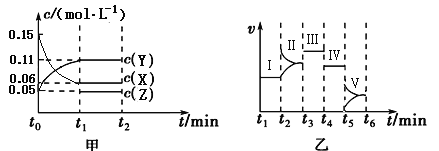
回答下列问题:
(1)若t1=5 min,则t0~t1阶段以X浓度变化表示的反应速率为v(X)= 。
(2)在t2~t3阶段Y的物质的量减小,则此阶段开始时v正 v逆(填“>”、“=”或“<”)。
(3)t4~t5阶段改变的条件为 ,此阶段的平衡常数K = 。
(4)t5~t6阶段容器内Z的物质的量共增加0.10 mol,在反应中热量变化总量为a kJ,写出该反应的热化学方程式 。在乙图Ⅰ~Ⅴ处平衡中,平衡常数最大的是 。
(5)若起始实验条件不变,重新向该容器中加入0.60 mol X、0.20 mol Y和0.080 mol Z,反应至平衡状态后X的转化率= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com