
| A. | 含0.1 molL-1SO2的溶液中:Na+、Ba2+、Br-、Cl- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Mg2+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液中:K+、NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | |
| D. | 不能使酚酞变红的无色溶液中:Na+、K+、ClO-、I- |
分析 A.含0.1 molL-1SO2的溶液呈酸性,离子之间不反应;
B.能与金属铝反应放出氢气的溶液可能为强碱性溶液或非氧化性酸溶液;
C.$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液呈碱性;
D.不能使酚酞变红的无色溶液可能呈酸性、中性或弱碱性.
解答 解:A.含0.1 molL-1SO2的溶液呈酸性,由于SO32-离子浓度较小,不生成沉淀,且其它离子之间不反应,可大量共存,故A正确;
B.能与金属铝反应放出氢气的溶液可能为强碱性溶液或非氧化性酸溶液,如呈酸性,不能生成氢气,如呈碱性,Mg2+不能大量共存,故B错误;
C.$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液呈碱性,NH4+不能大量共存,故C错误;
D.酚酞的变色范围为8~10,不能使酚酞变红的无色溶液可能呈酸性、中性或弱碱性,ClO-、I-发生氧化还原反应而不能大量共存,故D错误.
故选A.
点评 本题考查离子的共存,为高考常见题型,侧重信息的抽取和氧化还原反应及水解反应的考查,注重学生思维严密性的训练,有利于提高学生分析问题解决问题的能力,题目难度不大.


科目:高中化学 来源: 题型:解答题
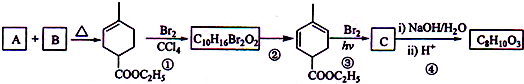
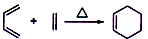
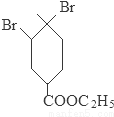 +2NaOH
+2NaOH
 +2NaBr+2H2O;
+2NaBr+2H2O;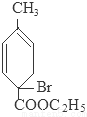 +2H2O
+2H2O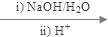
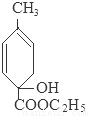 +C2H5OH+HBr:
+C2H5OH+HBr: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )
短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )| A. | 最简单气态氢化物的稳定性:X>Y | |
| B. | 单核阴离子半径:Z>W | |
| C. | 含Z元素的盐溶液可能显酸性、碱性或中性 | |
| D. | W元素的单质具有漂白性,常用于自来水的杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
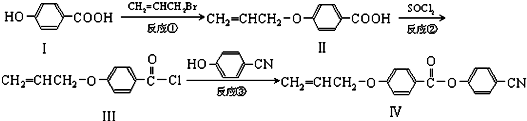
 .
. 也可与III发生类似反应③的反应,生成有机物V,V的结构简式是
也可与III发生类似反应③的反应,生成有机物V,V的结构简式是 .
.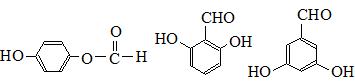 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O | |
| B. | 若乙池中为足量AgNO3溶液,则阳极的电极反应为:4OH--4e-═2H2O+O2↑ | |
| C. | 若乙池中为一定量CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为0.2NA | |
| D. | 常温常压下,1gCH3OH燃料生成CO2和液态H2O时放热22.68 kJ,表示该反应的热化学方程式为:CH3OH(l)+1.5O2(g)═CO2(g)+2H2O(l)△H=-725.76 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
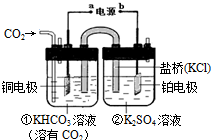
| A. | 该过程是电能转化为化学能的过程 | |
| B. | 铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O | |
| C. | 一段时间后,②池中溶液的pH一定增大 | |
| D. | 盐桥中K+移向铜电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
下列关于同系物的说法中,错误的是( )
A.同系物具有相同的最简式
B.同系物能符合同一通式
C.同系物中,相邻的同系物彼此在组成上相差一个CH2原子团
D.同系物的化学性质基本相似,物理性质随碳原子数增加而呈规律性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com