
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 2.1氨的合成练习卷(解析版) 题型:简答题
在氨的工业合成中,有三个关键的技术问题,请结合所学知识解决它们。
(1)合成氨的化学原理是N2+3H2??2NH3,在工业上选择20~50 MPa的较高压强和450 ℃左右的温度来进行反应,请结合有关的化学原理解释。
(2)在生产过程中需要大量氢气,现有以下几种获得氢气的方法,请你选出最适宜的,并说明理由。
A.电解水制取氢气
B.由煤或焦炭来制取氢气:煤或焦炭经加热,炽热的炭与水蒸气反应生成氢气
C.由天然气或重油制取氢气:天然气的主要成分甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳;一氧化碳在催化剂存在的条件下与水蒸气反应得到氢气和二氧化碳
(3)合成氨的生产工艺流程:首先用适当的方法生产出合成氨的原料气——氮气和氢气。氮气和氢气的混合气体在合成塔中于一定条件下,通过催化剂的作用产生氨气,再通过氨分离器不断地把生成的氨分离出来,同时未转化的反应气体再进入合成塔循环加工。这就是合成氨的工艺流程。请根据这一描述过程画出流程方框图。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年吉林省长春市高三第二次模拟考试(理综)化学部分 题型:填空题
(15分)
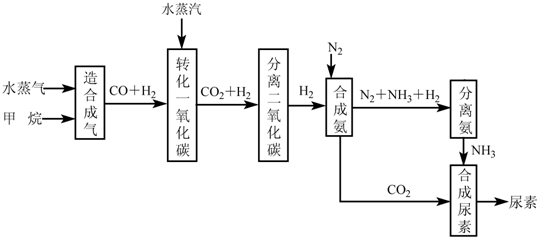
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某
些转化步骤及生成物未列出):

请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是: ______。
(2)上述流程中,工业上分离H2 、CO2合理的方法是___________。
A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行___________,目的是________________________________________;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法: 。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
查看答案和解析>>
科目:高中化学 来源: 题型:
在氨的工业合成中,有三个关键的技术问题,请结合所学知识解决它们:
(1)合成氨的化学原理是N2+3H2 ![]() 2NH3,在工业上选择20―50MPa的较高压强和 500
2NH3,在工业上选择20―50MPa的较高压强和 500![]() 的温度来进行反应,请结合有关的化学原理解释。
的温度来进行反应,请结合有关的化学原理解释。
(2)在生产过程中需要大量氢气,现有以下几种获得氢气的方法,请你选出最适宜的,并说明理由。
A.电解水制取氢气;B.由煤或焦碳来制取氢气:煤或焦碳经加热,炽热的炭与水蒸气反应生成氢气;C.由天然气或重油制取氢气:天然气的主要成分甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳,一氧化碳在催化剂存在的条件下与水蒸气反应得到氢气和二氧化碳。
(3)合成氨的生产工艺流程:首先用适当的方法生产出合成氨的原料气一一氮气和氢气。
氮气和氢气的混合气体在合成塔一定条件下,通过催化扭l的作用产生氨气,再通过氮分离器不断地把生成的氨分离出来,同时未转化的反应气体再进入合成塔循环加工。这就是合成氨的工艺流程。请根据这一描述过程画出流程方框图。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com