
【题目】四种基本反应类型中不可能设计成原电池的是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作_____剂。
(2)自然界Cr主要以+3价和+6价(Cr2O72-)存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。写出离子方程式:_____________________________
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是_________________________________。
(4)由铝土矿生产纯净的氧化铝,流程如下:
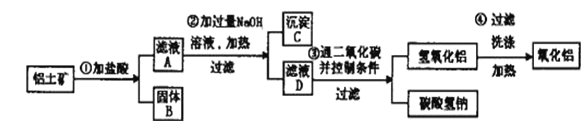
①第一步操作后,若在固体B中加入氢氧化钠溶液_______________(填”会”或”不会”)发生反应。
②验证滤液A中是否含Fe3 +,可取少量滤液A并加入____________(填试剂名称),现象是_________________________________。
③在整个操作过程中______________(填“是”或“否”)有氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下已知:4Al(s)+3O2(g)===2Al2O3(s) ΔH1 4Fe(s)+3O2(g)===2Fe2O3(s) ΔH2
下面关于ΔH1、ΔH2的比较正确的是( )
A. ΔH1>ΔH2 B. ΔH1<ΔH2 C. ΔH1=ΔH2 D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于燃烧热的说法正确的是
A. 燃烧反应放出的热量就是该反应的燃烧热
B. 1 mol可燃物质发生氧化反应所放出的热量就是燃烧热
C. 1 mol可燃物质完全燃烧生成稳定的化合物时所放出的热量就是燃烧热
D. 在25 ℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量是燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃相对分子质量为86,跟Cl2反应生成一氯取代物只有两种,它的结构简式、名称全正确的是( )
A. CH3(CH2)4CH3 己烷 B. (CH3)2CHCH(CH3)22,3-二甲基丁烷
C. (C2H5)2CHCH32-乙基丁烷 D. C2H5C(CH3)32,2-二甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W,X,Y,Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色.下列判断正确的是( )
A.金属性:Y>Z
B.氢化物的沸点:X>W
C.离子的还原性:X>W
D.原子及离子半径:Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电子式表示下列物质的结构:
(1)NH4Cl;
(2)Na2O;
(3)Na2O2;
(4)H2S;
(5)CO2;
(6)MgCl2;(1)~(6)中,仅含离子键的是 , 仅含共价键的是 , 既有离子键又有共价键的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) ![]() N2O4(g) ΔH<0,反应相同时间后,分别测定五个容器中NO2的百分含量(NO2%),并作出NO2%与对应不同温度的五个容器的关系图。下列示意图中,可能与实验结果相符的是( )
N2O4(g) ΔH<0,反应相同时间后,分别测定五个容器中NO2的百分含量(NO2%),并作出NO2%与对应不同温度的五个容器的关系图。下列示意图中,可能与实验结果相符的是( )

A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com