
下列离子方程式书写正确的是( )
A.将铜屑加入Fe3+溶液中:Fe3++Cu=Fe2++Cu2+
B.NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH- NH3↑+H2O
NH3↑+H2O
C.稀硝酸和过量的铁屑反应:
Fe+4H++NO3-=Fe3++NO↑+2H2O
D.KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+=I2+2H2O
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(三) (解析版) 题型:填空题
二氧化锰可用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。
(1)二氧化锰在酸性介质中是一种强氧化剂,请用化学方程式证明:______________________。
(2)锌—锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。电池的总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。
①电池工作时,MnO2发生________反应。
②电池的正极反应式为________。
(3)工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
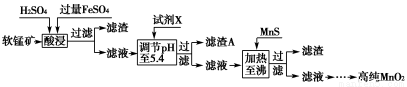
已知:软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物,部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表。
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 |
沉淀物 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
pH | 8.0 | -0.42 | 2.5 | 7 | 7 |
回答下列问题:
①硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为________________________。
②试剂X为________。
③滤渣A的主要成分为________。
④加入MnS的目的主要是除去溶液中的________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练3 元素及其化合物练习卷(解析版) 题型:选择题
下表中各组物质不能实现如图转化的是( )

选项甲乙丙
AAlCl3AlAl(OH)3
BAlCl3Al(OH)3NaAlO2
CCO2NaHCO3Na2CO3
DCO2(NH4)2CO3NH3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练2 化学基本理论练习卷(解析版) 题型:选择题
下列有关化学实验操作合理的是( )
①在配制FeSO4溶液时常向其中加入一定量铁粉和稀硫酸
②配制100 mL 1.00 mol/L的NaCl溶液时,可用托盘天平称取5.85 g NaCl固体
③物质溶于水的过程中,一般有放热或吸热现象,因此溶解的操作不能在量筒中进行
④用试管夹从试管底由下往上夹住距试管口约1/3处,手持试管夹长柄末端,进行加热
⑤不慎将浓硫酸沾在皮肤上,立即用NaHCO3溶液冲洗
⑥用广泛pH试纸测得某溶液的pH=12.3
⑦用碱式滴定管量取20.00 mL 0.100 0 mol/L KMnO4溶液
⑧将铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜
A.④⑤⑥⑦ B.①④⑤⑦ C.②③⑥⑧ D.①③④⑧
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练1 化学基本概念练习卷(解析版) 题型:填空题
食盐和工业用盐具有广泛的用途。已知工业用盐主要成分为NaNO2,外观酷似食盐并有咸味。NaNO2有氧化性和还原性,遇酸分解放出NO2。
(1)下列试剂可鉴别工业用盐和食盐的是________。
a.H2O b.硝酸酸化的硝酸银 c.盐酸
(2)NaNO2与氢碘酸反应(含氮产物为NO)的离子方程式为______________。
(3)某工厂废液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2中的氮转化为对空气无污染的气体,该物质是________。
a.NaCl b.NH4Cl c.浓H2SO4
(4)氯碱工业通过电解饱和食盐水来获得相应的产物。请写出电解食盐水的离子方程式______________________________________,
若在标准状况下生成3.36 L H2,则溶液中生成的OH-的物质的量为____。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练1 化学基本概念练习卷(解析版) 题型:选择题
下列化学用语表示正确的是( )
A.Cl-的结构示意图:
B.甲烷分子的球棍模型:
C.氢氧化钠的电子式: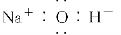
D.次氯酸的结构式:H—O—Cl
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后训练专题练习卷二(解析版) 题型:填空题
光伏并网发电并使用半导体(LED)照明可以节约大量能源。已知发出白光的LED是由氮化镓(GaN)芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的,如图所示。
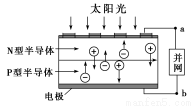
(1)砷与氮位于同主族,砷化镓也是半导体材料,它的化学式为________。
(2)用简单氧化物形式表示YAG的组成:________。
(3)下列有关光伏并网发电的叙述正确的是________(填序号)。
①LED是新型无机高分子材料
②电流从a流向b
③光伏电池是将太阳能直接转化为电能
④图中N型半导体为正极,P型半导体为负极
⑤如果工业上用光伏电池并网发电精炼粗铜,a极连接精铜电极
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后训练专题练习卷二(解析版) 题型:选择题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
A.放电时锌作负极
B.充电时氢氧化铁被氧化
C.放电时溶液的碱性增强
D.放电时转移3 mol e-,有2 mol FeO42-被还原
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练9-2练习卷(解析版) 题型:选择题
电解100 mL含c(H+)=0.30 mol·L-1下列溶液,当电路中通过0.04 mol
电子时,理论上析出金属质量最大的是( )
A.0.10 mol·L-1AgNO3溶液
B.0.10 mol·L-1ZnSO4溶液
C.0.20 mol·L-1CuCl2溶液
D.0.20 mol·L-1Pb(NO3)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com