
【题目】化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)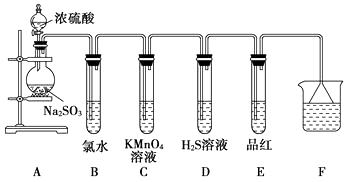
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是、。
(2)反应后,装置B中发生的现象是;反应的离子方程式为;装置C中的现象是 , 表现了SO2的;装置D中现象是 , 发生反应的化学方程式为。
(3)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象。
(4)F装置的作用是 , 漏斗的作用是。
【答案】
(1)分液漏斗,圆底烧瓶
(2)溶液褪色,SO2+Cl2+2H2O=4H++2Cl?+ ![]() ,溶液紫色褪去(溶液褪色),还原性,有黄色沉淀生成,2H2S+SO2=3S↓+2H2O
,溶液紫色褪去(溶液褪色),还原性,有黄色沉淀生成,2H2S+SO2=3S↓+2H2O
(3)将试管E在酒精灯上加热,溶液恢复红色
(4)吸收多余的SO2,防止倒吸
【解析】浓硫酸与Na2SO3发生反应Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O,SO2能使氯水及酸性KMnO4溶液褪色,在反应中SO2表现还原性;SO2与装置D中的H2S发生反应SO2+2H2S=3S↓+2H2O,从而使溶液变浑浊,该反应中SO2表现氧化性;SO2能使品红溶液褪色,但加热后溶液又恢复红色,说明SO2与品红溶液的作用具有可逆性;装置F用于吸收多余的SO2,因为SO2易与NaOH溶液反应,因此采用倒扣漏斗吸收SO2可防止液体倒吸。
根据实验室中制取二氧化硫的反应原理、二氧化硫的还原性和氧化性的实验,以及二氧化硫的漂白性和尾气处理方法进行解答即可.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A:
4HCl+O2  2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
ⅱ. 
(1)反应A的热化学方程式是 .
(2)断开1mol H﹣O键与断开1mol H﹣Cl键所需能量相差约为 kJ,H2O中H﹣O键比HCl中H﹣Cl键(填“强”或“弱”) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄金是一种贵重的金属。在人类漫长的历史上,黄金是许多人梦寐以求的,并有“沙里淘金”,“真金不怕火炼”之说。这说明黄金在自然界中主要以________形式存在,也说明黄金的化学性质在自然条件下非常________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol有机物与0.5mol O2恰好完全燃烧后的产物为CO2和H2O(g).产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过碱石灰剩余气体被完全吸收,碱石灰质量增加17.6g.
(1)燃烧后产物的物质的量分别为CO2mol、H2O(g)mol.
(2)推断该有机物的分子式为 .
(3)若0.2mol该有机物恰好与9.2g金属钠完全反应,其核磁共振氢谱显示只有两种不同环境的H,试确定该有机物的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是在人类文明发展过程中起了重要作用的元素。下列有关硅的说法正确的是( )
A. 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
B. 硅在自然界中有单质存在
C. 光纤通信是以光作为信息的载体,光导纤维的主要成分是SiO2
D. 硅单质的性质十分稳定,不能和任何物质发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,汉江流域再次发生“水华”现象,江面上有大量绿色漂浮物,类似于海面上的“红潮”,取水样分析:绿藻含量比正常情况下偏高很多,含氧量明显偏低,浑浊度增加。造成汉江“水华”最可能的原因是( )
A.水土流失
B.有毒的废水大量排入汉江
C.生活废水大量排入汉江,使水质富营养化
D.汉江流域农业生产中长期使用农药
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.100℃时,0.001molL﹣1的NaOH溶液pH=11
B.若溶液中c(H+)与c(OH﹣)相等,溶液肯定呈中性
C.25℃,0.001mol/LH2SO4溶液中,水电离出的c(OH﹣)为10﹣11mol/L
D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水资源非常重要,下列关于水的说法中错误的是( )
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0℃以上,温度越高,水的密度越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.NH3具有还原性,可用作制冷剂B.NaClO溶液显碱性,可用作杀菌消毒
C.浓硫酸具有吸水性,可用作干燥剂D.Al2O3具有两性,可用作耐高温材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com