
| ���ۼ� | H2���� | N2���� | NH3���� |
| ���ܣ�kJ?mol-1�� | 436 | 945 | 391 |
| ���� |
| ������ѹ |
| ���¸�ѹ |
| ���� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ţ���Ǵ�����������ڸ߷��� |
| B��ţ���Ǹ�֬����ĸ����� |
| C��ţ�Ϳ����ڼ��������¼���ˮ�� |
| D����ҵ�Ͻ�ţ�ͼ�������Ӳ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
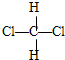 ��
��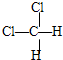 ��
��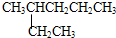 ��
�� 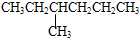
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������� |
| B����������������� |
| C����Һ������ |
| D����Һ����ɢϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼��þ����������Һ MgCO3+2H+�TMg2++H2O+CO2�� |
| B�������ʯ��ˮ��ϡ���ᷴӦ Ca��OH��2+2H+=Ca2++2H2O |
| C����������ϡH2SO4��� O2-+2H+=H2O |
| D��̼������ڴ����� CaCO3+2H+�TCa2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com