
(20分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。
I. 探究浓硫酸的某些性质
(1)按图示的连接装置,检查装置的气密性,称量E的质量;
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸;
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象:
写出A中发生反应的化学方程式___________________________________________(任写一个); B中的现象是________________________________________,由此可得到浓硫酸具有____________性;C中足量的酸性KMnO4溶液所起的作用是________________________;
D中盛放的试剂是_______________。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式:
___________________________________(任写一个)。
Ⅱ.测定铁的质量分数
(5)待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g,则铁碳合金中铁的质量分数为:___________________________________________(写表达式);
某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是_____________________________________________________________________;
(6)经过大家的讨论,决定采用下列装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量
⑶2Fe+6H2SO4(浓)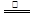 Fe2(SO4)3+3SO2↑+6H2O(或C+2H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O(或C+2H2SO4(浓)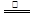 CO2↑+2SO2↑+2H2O)(2分); 品红溶液逐渐褪色(2分); 强氧化(2分); 除去CO2中混有的SO2(2分);浓硫酸(2分);
CO2↑+2SO2↑+2H2O)(2分); 品红溶液逐渐褪色(2分); 强氧化(2分); 除去CO2中混有的SO2(2分);浓硫酸(2分);
⑷2Fe3++Fe=3Fe2+(或Fe+2H+=Fe2++H2↑,SO2+2Fe3++2H2O=2Fe2++SO42-+4H+)(2分);
⑸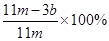 (或
(或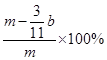 (3分)); 空气中CO2、H2O进入E管使b增大(2分)
(3分)); 空气中CO2、H2O进入E管使b增大(2分)
⑹③(3分)
解析试题分析:(3)浓硫酸具有强氧化性,能和铁或碳在加热的条件下反应,反应的化学方程式是2Fe+6H2SO4(浓)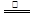 Fe2(SO4)3+3SO2↑+6H2O、C+2H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O、C+2H2SO4(浓)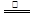 CO2↑+2SO2↑+2H2O。SO2具有漂白性,能使品红溶液褪色,所以B中的实验现象是品红溶液逐渐褪色,这说明浓硫酸被还原生成了SO2,因此说明浓硫酸具有强氧化性。由于SO2也是一种酸性氧化物,能干扰CO2的检验,所以酸性高锰酸钾溶液的作用是除去CO2中混有的SO2。由于碱石灰也能吸收水蒸气,所以D装置的作用是干燥CO2气体,所以盛放的试剂是浓硫酸。
CO2↑+2SO2↑+2H2O。SO2具有漂白性,能使品红溶液褪色,所以B中的实验现象是品红溶液逐渐褪色,这说明浓硫酸被还原生成了SO2,因此说明浓硫酸具有强氧化性。由于SO2也是一种酸性氧化物,能干扰CO2的检验,所以酸性高锰酸钾溶液的作用是除去CO2中混有的SO2。由于碱石灰也能吸收水蒸气,所以D装置的作用是干燥CO2气体,所以盛放的试剂是浓硫酸。
(4)由于随着反应的进行,稀硫酸的浓度会逐渐降低,所以有可能生成氢气。另外如果铁过量,则氯化铁还可能氧化剩余的单质铁,同时也可能氧化生成的SO2气体,因此可能的离子方程式是2Fe3++Fe=3Fe2+(或Fe+2H+=Fe2++H2↑,SO2+2Fe3++2H2O=2Fe2++SO42-+4H+)。
(5)E装置增加的质量就是CO2的质量,所以根据碳原子守恒可知,碳的质量是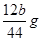 ,则则铁碳合金中铁的质量分数
,则则铁碳合金中铁的质量分数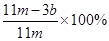 。由于空气中含有水蒸气和CO2,也会加入E装置中,导致b偏大,所以测定结果偏低。
。由于空气中含有水蒸气和CO2,也会加入E装置中,导致b偏大,所以测定结果偏低。
(6)由于气体的体积测量往往受温度和压强的影响,不易测量,①不正确,②态复杂。在反应中碳和稀硫酸不反应,只有铁和稀硫酸反应生成氢气和硫酸亚铁,所以可以根据质量守恒定律,常用实验③。
考点:考查浓硫酸的性质、方程式的书写、物质的检验、质量分数的计算等
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。探究性实验的一般思路是:1.准确地把握实验目的;2.利用已学知识,分析如何实现这个目的--实验原理;3.结合实验材料,初步确定设计对策--实验方案。


科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
| 11m-3b |
| 11m |
| 11m-3b |
| 11m |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 11m-3b |
| 11m |
| 11m-3b |
| 11m |
m-
| ||
| m |
m-
| ||
| m |
 (5)经过大家的讨论,决定采用下图装置(干燥管中试剂为无水氯化钙,锥形瓶中为mg铁炭合金和足量稀硫酸.)和其他常用实验仪器测定某些数据即可.为了快速测算出铁的质量分数,最简便的实验操作是
(5)经过大家的讨论,决定采用下图装置(干燥管中试剂为无水氯化钙,锥形瓶中为mg铁炭合金和足量稀硫酸.)和其他常用实验仪器测定某些数据即可.为了快速测算出铁的质量分数,最简便的实验操作是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com