
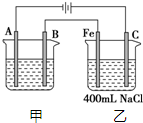
 如图所示为相互串联的甲、乙两电解池.试回答:
如图所示为相互串联的甲、乙两电解池.试回答:分析 根据电源的正负极可判断A、B、Fe、C分别为电解池的阴极、阳极、阴极、阳极,在阴极上发生还原反应,在阳极上发生氧化反应,乙池反应中阴极:2H2O+2e-═H2↑+20H-,阳极:2Cl--2e-═Cl2↑,若甲为用电解原理给铁片镀银的装置,阴极反应为Ag++e-=Ag,阳极反应为Ag-e-=Ag+,电解质溶液应选与镀层具有相同金属离子的可溶性盐溶液;然后根据电极反应以及两个串联电解池转移电子数目相等计算.
解答 解:(1)根据电源的正负极可判断A、B、Fe、C分别为电解池的阴极、阳极、阴极、阳极,在阴极上发生还原反应,在阳极上发生氧化反应,在铁片上镀银时,镀层金属银为电解池的阳极,阳极上的电极反应式为Ag-e-=Ag+,镀件金属铁为电解池的阴极,阴极上的电极反应式Ag++e-=Ag,电解质溶液含有镀层金属离子,应为可溶性硝酸银溶液.
故答案为:阴极;Ag++e-=Ag;银; Ag-e-=Ag+;AgNO3;
(2)乙池电解NaCl溶液,阴极反应为:2H2O+2e-═H2↑+20H-,总反应的离子方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2+H2+2OH-,滴加酚酞溶液后,阴极溶液变红.阳极反应式为:2Cl--2e-═Cl2↑,放氢生成碱型,所以溶液的PH值变大,生成氢气和氯气,所以要使溶液复原应加入只要通入氯化氢气体,
故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2+H2+2OH-;红;变大;HCl;
(3)甲槽阴极反应为Ag++e-=Ag,阴极增重4.32g,应为银的质量,n=$\frac{4.32g}{108g/mol}$=0.04 mol,
转移的电子为0.04mol,两个电解池串联,转移的电子数目相等,乙槽阳极反应为2Cl--2e-═Cl2↑,
转移的电子为0.04mol时,在阳极上生成气体的物质的量为0.02mol,
放出气体在标准状况下的体积为0.02mol×22.4L/mol=0.448L=448mL,
设氢氧化钠的物质的量为x.
2NaCl+2H2O=Cl2↑+2NaOH+H2↑ 转移电子
2mol 2mol
x 0.04mol
所以x=0.04mol
氢氧化钠的物质的量浓度C=$\frac{0.04mol}{0.4L}$=0.1mol/L,C(H+ )=$\frac{1×1{0}^{-14}}{0.1}$=1×10-13mol/L
所以溶液的PH值为13.
故答案为:448;13.
点评 本题考查了电镀原理及氧化还原反应的有关计算,难度不大,注意串联电解池得失电子数相等的特点.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 得电子越多,其氧化性越强 | |
| B. | 阳离子只有氧化性,阴离子只有还原性 | |
| C. | 要完成SO32-→SO42-的转化,必须加入氧化剂 | |
| D. | 金属活动顺序表中,排在前面的金属阳离子的氧化性强于排在后面的金属阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe分别与氯气和稀盐酸反应所得氯化物相同 | |
| B. | 常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 | |
| C. | 氯气具有漂白性 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数大于4的元素不一定是非金属元素 | |
| B. | 同周期的主族元素从左到右,非金属性逐渐增强,气态氢化物稳定性逐渐减弱 | |
| C. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素不一定是金属元素 | |
| D. | 核外电子排布完全相同的两种微粒,其化学性质一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向100mL0.1mol•L-1的Na2CO3溶液中滴加含0.01molCH3COOH的醋酸溶液CO32-+CH3COOH═HCO3-+CH3COO- | |
| B. | 4mol•L-1的NaAlO2溶液和7mol•L-1的盐酸等体积均匀混合4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 等物质的量的FeBr2与Cl2反应(已知:Br2+2Fe2+═2Fe3++2 Br-,Cl2+2Br-═Br2+2Cl-):2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向NaAlO2溶液中通入过量CO2的反应:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6 | B. | C2H6O | C. | C2H6O2 | D. | C3H6O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com