
| A. | 放热反应,熵增加 | B. | 放热反应,熵减小 | C. | 吸热反应,熵增加 | D. | 吸热反应,熵减小 |
分析 化学反应能否自发进行,取决于焓变和熵变的综合判据,当△G=△H-T•△S<0时,反应能自不发进行.
解答 解:依据焓变和熵变的综合判据:△H-T•△S,
当:△H<0,△S>0,即放热反应,熵增加,△H-T•△S<0一定成立,反应在所有温度下都能自发进行;
△H>0,△S<0,即吸热反应,熵减小,△H-T•△S<0一定不成立,反应一定不能自发进行;
△H<0,△S<0,即放热反应,熵减小,△H-T•△S<0在低温一定成立,低温下能够自发进行;
△H>0,△S>0,即吸热反应,熵增加,△H-T•△S<0在高温一定成立,高温下能够自发进行;
故选:A.
点评 本题考查了反应自发进行方向的判断,明确焓变和熵变的综合判据是解题关键,题目难度不大.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 同素异形体:是否由同一种原子构成 | |
| B. | 纯净物和混合物:是否只含一种元素 | |
| C. | 电解质和非电解质:溶于水或熔融状态下能否导电 | |
| D. | 氧化还原反应:元素化合价是否变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L SO3中含有0.5NA个SO3分子 | |
| B. | 48g O3气体含有3NA个氧原子 | |
| C. | 在1L0.5mol•L-lFeCl3溶液中含有0.5NA个Fe3+ | |
| D. | 1.5 mol NO2与足量水反应,转移的电子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
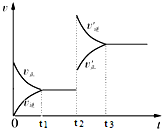 向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t2时刻改变反应的某一条件(混合气体总物质的量不变),速率变化如图所示,则下列说法正确的是( )
向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t2时刻改变反应的某一条件(混合气体总物质的量不变),速率变化如图所示,则下列说法正确的是( )| A. | 重新达到平衡后,平衡常数K增大 | B. | t2时刻改变的条件可以是升高温度 | ||
| C. | I2(g)转化率增大,HI平衡浓度增大 | D. | t2时刻改变是可以增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:PH3>H2S>HCl | B. | 酸性:HClO4>HBrO4>HIO4 | ||
| C. | 非金属性:F>O>S | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com