
| A. | 反应C(s)+H2O(g)?CO(g)+H2(g) 的平衡常数为:K=$\frac{c(CO)•c({H}_{2})}{c(C)•c({H}_{2}O)}$ | |
| B. | 反应Cr2O72-+H2O?2CrO42-+2H+ 的平衡常数为:K=$\frac{c(Cr{O}_{4}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{O}_{3}^{2-})•c({H}_{2}O)}$ | |
| C. | NH4++H2O?NH3•H2O+H+的平衡常数为:K=$\frac{{K}_{W}}{{K}_{b}(N{H}_{3}•{H}_{2}O)}$ | |
| D. | 2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq)的平衡常数为:K=$\frac{{K}_{sp}(A{g}_{2}S)}{{{K}_{sp}}^{2}(AgI)}$ |
分析 A.平衡常数表达式中不用管它或纯液体;
B.水为纯液体,平衡常数表达式中不写入;
C.铵根水解平衡常数、电离平衡常数、离子积常数的代换计算分析判断;
D.Ksp(Ag2S)=c2(Ag+)c(S2-),Ksp(AgI)=c(Ag+)c(I-),结合沉淀转化的平衡常数计算分析判断.
解答 解:A.反应C(s)+H2O(g)?CO(g)+H2(g),反应中碳为固体,所以反应的平衡常数K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$,故A错误;
B.反应Cr2O72-+H2O?2CrO42-+2H+ 中水为纯液体,平衡常数为:K=$\frac{{c}^{2}(Cr{{O}_{4}}^{2-}){c}^{2}({H}^{+})}{C(C{r}_{2}{{O}_{7}}^{2-})}$,故B错误;
C.NH4++H2O?NH3•H2O+H+的平衡常数为:K=$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}$=$\frac{c(N{H}_{3}•{H}_{2}O)c({H}^{+})}{c(N{{H}_{4}}^{+})}$×$\frac{c(O{H}^{-})}{c(O{H}^{-})}$=$\frac{Kw}{Kb(N{H}_{3}•{H}_{2}O)}$,故C正确;
D.2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq)的平衡常数K=$\frac{{c}^{2}({I}^{-})}{c({S}^{2-})}$=$\frac{{c}^{2}({I}^{-})}{c({S}^{2-})}$×$\frac{{c}^{2}(A{g}^{+})}{{c}^{2}(A{g}^{+})}$=$\frac{Ks{p}^{2}(AgI)}{Ksp(A{g}_{2}S)}$,故D错误;
故选C.
点评 本题考查平衡常数概念的理解应用、表达式书写方法,主要是平衡常数变化形式和离子积常数、电离平衡常数、溶度积常数等的计算,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
| B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该食盐中一定没有添加KIO3 |
| D | 向Na2SiO3溶液中滴加乙酸溶液 | 溶液变浑浊 | 相同条件下,乙酸的酸性一定比硅酸强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
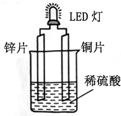
| A. | 铜片表面有气泡生成 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 如果将铜片换成铁片,电路中的电流方向将改变 | |
| D. | 如果将铜片换成银片,LED灯仍正常发光 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
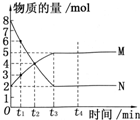 一定温度下,在容积为VL的密闭容器中进行反应:aN(g)═bM(g),M、N的物质的量随时间的变化曲线如图所示.
一定温度下,在容积为VL的密闭容器中进行反应:aN(g)═bM(g),M、N的物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:推断题



 的路线如下:
的路线如下:
 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
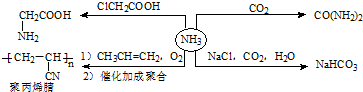
| A. | H2NCH2COOH是一种氨基酸 | |
| B. | CO(NH2)2与NH4CNO性质相同 | |
| C. | 聚丙烯腈的单体为:CH2═CHCN | |
| D. | 依据酸碱质子理论,HCO3-属于酸碱两性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
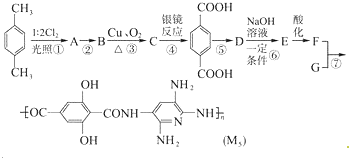
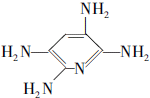 ,F的含氧官能团的名称有羧基、(酚)羟基.
,F的含氧官能团的名称有羧基、(酚)羟基.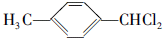 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
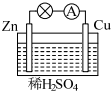 如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )
如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )| A. | ①②③ | B. | ②④⑥ | C. | ③④⑤ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com