
【题目】经X射线研究证明PCl5在固态时,其空间构型分别是正四面体和正八面体的两种离子构成,下列关于PCl5的推断正确的是( )
A.PCl5晶体是分子晶体
B.PCl5晶体由[PCl3]2+和[PCl2]2-构成,且离子数目之比为1∶1
C.PCl5晶体由[PCl4]+和[PCl6]-构成,且离子数目之比为1∶1
D.PCl5晶体具有良好的导电性
【答案】C
【解析】
![]() 在固体状态时,由空间构型分别为正四面体和正八面体两种离子构成,在杂化轨道理论中,正四面体构型的粒子只有
在固体状态时,由空间构型分别为正四面体和正八面体两种离子构成,在杂化轨道理论中,正四面体构型的粒子只有![]() 型,正八面体只有
型,正八面体只有![]() 型,结合该固体状态化学式知,
型,结合该固体状态化学式知,![]() 晶体由
晶体由![]() 和
和![]() 构成,据此分析解答。
构成,据此分析解答。
A.![]() 在固体状态时,由空间构型分别为正四面体和正八面体两种离子构成,所以其构成微粒是阴阳离子,为离子晶体,A项错误;
在固体状态时,由空间构型分别为正四面体和正八面体两种离子构成,所以其构成微粒是阴阳离子,为离子晶体,A项错误;
B.在杂化轨道理论中,正四面体构型的粒子只有![]() 型,正八面体只有
型,正八面体只有![]() 型,结合该固体状态化学式知,
型,结合该固体状态化学式知,![]() 晶体由
晶体由![]() 和
和![]() 构成,在离子化合物中,阴阳离子所带电荷相等,所以阴阳离子数目之比为1:1,B项错误;
构成,在离子化合物中,阴阳离子所带电荷相等,所以阴阳离子数目之比为1:1,B项错误;
C.根据B项分析![]() 晶体由
晶体由![]() 和
和![]() 构成,C项正确;
构成,C项正确;
D.根据分析,该物质是一个离子晶体,离子晶体在水溶液或熔融状态下能导电,在固体时没有自由移动离子而不能导电,D项错误;
答案选C。


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】某化学实验小组同学用如图所示装置进行系列实验,以探究气体的性质(部分仪器已略去)。
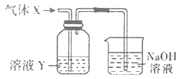
回答下列问题:
(1)若气体X为氯气,溶液Y为含有少量KSCN的FeCl2溶液,则可观察到溶液Y中的实验现象是___,写出NaOH溶液中发生反应的离子方程式:___。
(2)若溶液Y为品红溶液,气体X通过后,溶液褪色。取少量褪色后的溶液加热后恢复为红色,则气体X可能是___(填化学式)。根据气体X的性质,上述实验装置应作一定的改进,则下列装置中可用来替代其尾气吸收装置的是___(填序号)。
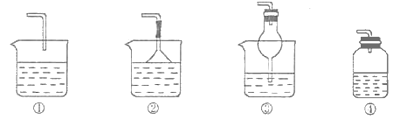
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将![]() 和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
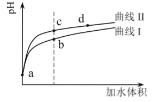
A.曲线Ⅰ代表HNO2溶液
B.溶液中水的电离程度:b点>c点
C.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
D.c点到d点,溶液中![]() 保持不变(HA、A-代表相应的酸和酸根离子)
保持不变(HA、A-代表相应的酸和酸根离子)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测被德国化学家合成证实。[18]-轮烯是一种大环轮烯,其结构简式如图所示。 有关它的说法正确的是

A.[18]- 轮烯分子中所有原子不可能处于同一平面
B.[18]- 轮烯的分子式为:C18H12
C.1 mol[18]- 轮烯最多可与9 mol氢气发生加成反应生成环烷烃
D.[18]- 轮烯与乙烯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X(s)+3Y(g)![]() Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将2mol X和2 mol Y通入2L的恒容密闭容器中,反应10s,测得生成0.5molZ。下列说法正确的是
Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将2mol X和2 mol Y通入2L的恒容密闭容器中,反应10s,测得生成0.5molZ。下列说法正确的是
A.10s内,X的平均反应速率为0.025 mol·Lˉ1·sˉ1
B.第10s时,Y的反应速率为0.075 mol·Lˉ1·sˉ1
C.第10s时,X为 1.5 mol,Y的浓度为0.25 mol·Lˉ1
D.10s内,X和Y反应放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】28g CO气体在1mol的氧气中燃烧后,所得的气体通过足量Na2O2固体中充分反应后,下列说法不正确的是( )
A. CO与氧气反应,只消耗了0.5mol氧气
B. 充分反应后Na2O2固体质量增加了28 g
C. 通过以上两步反应后余下氧气物质的量为0.5mol
D. 若2gH2替代 28g的CO发生上述反应,则Na2O2固体质量增加了2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是__________。
②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________、________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是_______________。
②E处干燥管中盛放的药品是碱石灰,其作用是_____________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量_____________(填“偏大”“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+……,然后测定其质荷比。某有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )
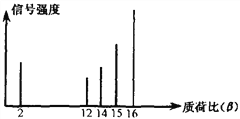

A. 甲醇 B. 丙烷 C. 甲烷 D. 乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态Co原子价电子排布图为______________(轨道表达式)。第四电离能I4(Co)比I4(Fe)小,是因为_____________________。
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是_________________________.
(3)乙炔(C2H2)分子中δ键与π键的数目之比为_______________。
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯( )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是___________;与该阴离子互为等电子体的分子有_____________。(列一种)
②碳酸亚乙酯分子中碳原子的杂化方式有_______________________。
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。

①S2-的配位数为______________。
②设NA为阿伏加德罗常数的值,Li2S的晶胞密度为____________(列出计算式)![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com