
【题目】下图是几种有机物的转换关系,请按要求填空:

已知:A是来自石油的重要有机化工原料,对水果有催熟作用;75%的B可用于医用消毒;E是 具有果香味的有机物,结构简式为C4H8O2;F是一种高聚物,可制成多种包装材料。
(1)G的名称是_____________; F的链节是_____
(2)反应类型:①__________; ③_____
(3)书写反应方程式: ②_____
(4)下列关于 A 和 F 的叙述正确的是_____
A.A 常温下是气体,为纯净物;F 常温下是固体,为混合物
B.A 和 F 都能使酸性高锰酸钾溶液褪色
C.取等质量的 A 和 F 完全燃烧后,生成的 CO2 和 H2O 的质量分别相等
D.取等物质的量的 A 和 F 完全燃烧后,生成的 CO2 和 H2O 的物质的量分别相等
(5)与 E 互为同分异构体,且含有“—COO—”结构的有机物还有____________种。
【答案】 1,2—二溴乙烷 —CH2—CH2— 加成反应 酯化反应 2 CH3CH2OH+ O2 ![]() 2 CH3CHO + 2H2O A、C 5
2 CH3CHO + 2H2O A、C 5
【解析】A是来自石油的重要有机化工原料,对水果有催熟作用,则A为CH2=CH2;75%的B可用于医用消毒,B为乙醇,A和水发生加成反应生成B为CH3CH2OH;B被催化氧化生成C为CH3CHO,A和溴发生加成反应生成G为CH2BrCH2Br;F是一种高聚物,可制成多种包装材料,则F为![]() ;E是具有果香味的有机物,B为酸性高锰酸钾溶液氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3。
;E是具有果香味的有机物,B为酸性高锰酸钾溶液氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3。
(1)G为CH2BrCH2Br,G的名称是 1,2-二溴乙烷,F为聚乙烯,链节是-CH2-CH2-,故答案为: 1,2-二溴乙烷;-CH2-CH2-;
(2)根据分析,反应①为乙烯与水的加成反应;反应③为乙醇和乙酸的酯化反应,故答案为:加成反应; 酯化反应;
(3)反应②为乙醇的催化氧化,反应的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO + 2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO + 2H2O,故答案为:2CH3CH2OH+O2![]() 2CH3CHO + 2H2O;
2CH3CHO + 2H2O;
(4)A为乙烯,F为聚乙烯。A.乙烯常温下为气体,属于纯净物,聚乙烯,常温下是固体,聚合度不同,属于混合物,故A正确;B.聚乙烯没有碳碳双键,不能使酸性高锰酸钾溶液褪色,故B错误;C.乙烯与聚乙烯的最简式相同,等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等,故C正确;D.乙烯与聚乙烯分子中含有碳原子数目不同、氢原子数目不同,取等物质的量的乙烯和聚乙烯完全燃烧后,生成的CO2的物质的量不相等,生成H2O的物质的量也不相等,故D错误,故选AC;
(5)E为CH3COOCH2CH3,与E互为同分异构体,且含有“—COO—”结构的有机物还有HCOOCH2CH2CH3,HCOOCH2(CH3)2,CH3CH2COOCH3,CH3CH2CH2COOH,(CH3)2CHCOOH,共5种,故答案为:5。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
【题目】某氮肥厂氨氮废水中的氮元素多以NH4+和NH3· H2O的形式存在,该废水的处理流程如下:
![]()
(1)过程I:加NaOH溶液,升温至60 ℃,调节pH至9后,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:_____________________。
②用化学平衡原理解释通空气的目的:_____________________。
③回收的氨气经净化处理后可进行催化氧化,已知催化剂为Cr2O3。
i.氨催化氧化的化学方程式为____________________。
ii.预先将催化剂加热到红热状态,停止加热后催化剂仍保持红热,该反应是______反应。
(填“吸热”或“放热”)
(2)过程II:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。请完成第一步反应的离子方程式:__________________________________________
(3)过程III:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 gCH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是
①天然气 ②煤 ③石油 ④太阳能 ⑤风能 ⑥氢能
A. ①②③ B. ①④⑤ C. ④⑤⑥ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活,生产密切相关,下列说法正确的是( )
A. 向燃煤中加入CaO、推广电动公交车均符合绿色化学理念
B. 市售“锌强化酱油”中含有大量锌元素
C. 银氨溶液常用于测定血液中葡萄糖的含量
D. 皂化反应用于制备高级脂肪酸和甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.回答下列有关双氧水的问题: 
(1)下述反应中,H2O2仅体现氧化性的反应是(填代号) .
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(2)保存过氧化氢的试剂瓶上最适合贴上的一个标签是(填代号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验是学习理解化学知识的基础,它以其生动的魅力和丰富的内涵在化学学习中发挥着独特的功能和作用。请回答下列问题:
I .实验室欲用固体NaOH配制100 mL 1mol·L-1的NaOH溶液。
(1)配制上述溶液,下列不能用到的仪器是____________________(用序号回答)。
A.烧杯 B.大试管 C.胶头滴管 D.100 mL容量瓶
(2)除上述仪器外,还一定要的玻璃仪器有______________。
(3)用托盘天平称取NaOH固体的质量为_________g,从下表中选择称量NaOH固体所需要的仪器 __________________(填序号)。

(4)下列情况使所配得溶液的浓度如何变化?(填“偏高”“ 偏低”或“不变”)
A.未洗涤溶解氢氧化钠的烧杯_________。
B.容量瓶使用前用蒸馏水洗过,内壁附有水珠而未干燥处理___________。
C.定容时加水超过了刻度线,将多出的液体吸出___________。
D.定容时俯视容最瓶读数___________。
II.已知化合物甲和乙都不溶于水,甲可溶于质最分数大于或等于98%的浓硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器,甲与硫酸不发生化学反应)。
请填写下列空白,完成由上述混合物得到固体甲的实验设计。
序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
① | 溶解 | 将混合物放入烧杯中,加入98% H2SO4____。 |
② | _____________ | |
③ | 稀释(沉淀) | ____________ |
④ | 过滤 | |
⑤ | _________ | 向④的过滤器中注入少量蒸馏水,使水面浸过沉淀物,待水滤出后,再次加水洗涤,连洗几次。 |
⑥ | 检验沉淀是否洗净 | ____________________。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中通入SO2,其中SO2的作用与SO2使酸性KMnO4溶液褪色原理相同的是
A. 溴水溶液褪色B. 品红溶液褪色C. NaOH酚酞溶液褪色D. 石蕊溶液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用铬铁矿(FeO![]() Cr2O3)冶炼铬的工艺流程如下:
Cr2O3)冶炼铬的工艺流程如下:

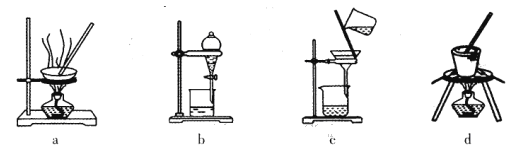
(1)实验室焙烧铬铁矿可选用的装置是__________(填序号)。
(2)完成下列化学方程式(在横线上填写物质的化学式及计量数):4CrO42-+6S+7H2O=4Cr(OH)3↓+3S2O32-+_____________。
(3)操作I包括过滤与洗涤,过滤需要的玻璃仪器有:__________________________。
(4)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物,写出Cr(OH)3溶于氢氧化钠溶液的
离子方程式_________________________________。
(5)由Cr2O3冶炼Cr的化学方程式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com