
| A. | 凡金属元素与非金属元素化合时都能形成离子键 | |
| B. | 非金属原子间不可能形成离子键 | |
| C. | 钠原子与氯原子通过得失电子,以离子键结合成氯化钠后体系能量降低 | |
| D. | 含有共价键的化合物一定是共价化合物 |
分析 A.氯化铝中只存在共价键;
B.铵盐中存在离子键;
C.氯化钠中只含离子键,形成化学键释放能量;
D.离子化合物中可能含共价键.
解答 解:A.氯化铝中只存在共价键,氯化铝由金属元素和非金属元素组成,故A错误;
B.铵盐中存在离子键,铵盐中只有非金属元素,故B错误;
C.氯化钠中只含离子键,形成化学键释放能量,则钠原子与氯原子通过得失电子,以离子键结合成氯化钠后体系能量降低,故C正确;
D.离子化合物中可能含共价键,如NaOH为含共价键的离子化合物,则含共价键的不一定为共价化合物,故D错误;
故选C.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 加热能杀死流感病毒是因为病毒的蛋白质受热发生变性 | |
| B. | 在豆浆中加少量石膏,能使豆浆凝结为豆腐 | |
| C. | 蛋白质水解的最终产物是氨基酸 | |
| D. | 任何结构的蛋白质遇到浓硝酸都会变成黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式为CH2=CH2 | B. | CH4分子的比例模型: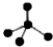 | ||
| C. | 8个中子的碳原子的符号:12C | D. | 氯化镁的电子式: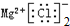 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| D. | 用Pt电极电解饱和氯化镁溶液:2Cl-+2H2$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 均是被腐蚀的金属失去电子的过程 | |
| B. | 均是需要有氧气参加的反应 | |
| C. | 化学腐蚀与电化学腐蚀往往是同时发生的 | |
| D. | 电化学腐蚀比化学腐蚀的速率通常情况下大得多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
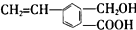 ,关于M的说法正确的是( )
,关于M的说法正确的是( )| A. | M中只有两种官能团 | |
| B. | 1 molM最多能消耗2 mol NaOH | |
| C. | M能使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色 | |
| D. | M可以发生酯化、加成反应,不能发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③⑤⑥⑦ | C. | 只有①⑦ | D. | ③⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com